上海市浦东新区康安路388弄2号615单元
朴衡博迈(上海)生物医药有限公司
朴衡博迈(上海)生物医药有限公司(PUHENG BIOMEDICINE)是一家专注于新型体外3D器官/疾病模型(包括NAC-Organ、类器官、器官芯片等复杂3D模型)研发和应用的创新型企业。企业自主研发的NAC-Organ技术是全球首个基于纳米核酸材料的组装式体外3D型构建及培养术,可快速实现人源化复杂器官/疾病模型的高通量、标准化生产。公司已建立以慢性肝病为特色的常见慢病、多种肿瘤、重要生理器官及多器官复合模型的建模技术打造了图形分析、免疫组化、分子生物学、病理学、AI预测等全方位检测平台及多维度的评价体系,成功为国内外知名大学、医院、科研院所、药企等提供高效、精准、严懂的科研服务,获得业界的高度认可。
-
体外3D复杂疾病模型开发
-
基于体外3D模型的药物检测
-
再生医学技术研发
引领技术创新和产业变革
-
国际领先的生物材料技术
NAC-linker是朴衡科技基于合成生物学技术开发的细胞连接材料,能够介导细胞实现三维空间的高效自组装,并实现细胞类型、数量和空间分布的精准调控。
-
10余种体外3D生理/病理模型
NAC-Organ技术仅需24小时即可制备包含肝实质细胞与非实质细胞的体外3D肝脏模型 (NAC-Liver)。 NAC-Liver能够在体外稳定培养超过30天,并且高水平的维持肝实质细胞的分泌、代谢等功能。
-
BT+AI的高效药物开发经验
为NAC-organ开发的自动化培养系统,能够实现3D模型的高通量自动培养与检测,保证模型的标准化和检测结果的可重复性。利用高内涵成像系统能够在NAC-organ上完成药效的高通量分析,进行细胞动态的实时监测。
新闻动态
成果解读 | 从靶点发现到机制验证,3D肝脏模型如何赋能肝纤维化疾病研究与新药研发
肝纤维化是各类慢性肝病进展为肝硬化、肝癌的核心病理枢纽,目前全球尚无获批可逆转病程的根治性药物,其复杂细胞互作网络与关键调控靶点仍待深入解析。酪氨酸激酶受体B(TrkB)在肝脏疾病中作用显著,团队前期已证实其可抑制肝星状细胞活化以发挥抗纤维化效应,但其在肝细胞——主导肝脏稳态的主要实质细胞——中的功能意义仍不充分。 近日,复旦大学附属中山医院董玲、姚群燕及朱长锋研究团队在《Cell Proliferation》在线发...
文献分享|研究揭示 ATF4 通过增强子程序调控肝星状细胞活化与 ECM 沉积
肝纤维化(Liver Fibrosis)作为非酒精性脂肪肝(NAFLD)、酒精性肝病、病毒性肝炎等多种肝损伤的共同病理结局,表现为肝内细胞外基质(ECM)过度沉积,并呈进行性发展,若不及时干预,将进一步进展为不可逆的肝硬化甚至原发性肝癌(HCC)。肝脏的天然修复机制中,肝星状细胞(HSCs)是核心的纤维化效应细胞。正常状态下 HSCs 呈静息态,储存脂质。当肝组织受损时,HSCs 被激活并转分化为肌成纤维细胞样细胞...
文献分享|脂肪来源SVF自组装“多功能骨类器官”:成骨、血管化、免疫调节三位一体,破解骨修复难题!
骨骼是人体的支撑核心,但大骨缺损、骨折不愈合、骨坏死等复杂骨科疾病,一直是临床治疗的棘手难题。传统骨移植疗法存在显著局限:自体骨供区有限、手术创伤大,异体骨易引发免疫排斥,而单纯干细胞移植又难以解决血管化不足、炎症微环境失衡等问题。 近年来,类器官技术与骨组织工程的结合为治疗带来新希望。脂肪组织来源的基质血管部分(SVF),因获取便捷、细胞成分丰富,成为骨类器官构建的潜力细胞源。它包含脂肪间充质干细...
成果解读:人源化肝类器官助力肝缺血再灌注损伤(IRI)研究
肝缺血再灌注损伤(ischemia-reperfusion injury, IRI)是肝切除、肝移植等重大手术后导致肝功能障碍甚至衰竭的核心病理基础之一。然而,由于IRI过程高度依赖肝实质细胞、非实质细胞及免疫细胞之间的复杂互作,长期以来,缺乏真正“接近人体真实肝脏”的体外模型,严重制约了机制研究与药物筛选。 传统二维细胞模型过于简化,动物模型又存在显著的物种差异,尤其在免疫反应和信号通路层面,难以精准预测人类临床结果。如何在体外...
重磅消息!美国疾病控制与预防中心的科学家已被告知逐步停止所有猴子研究!
近日,《科学》杂志披露的一则重磅消息在全球生物医学界引发巨大震动:美国疾病控制与预防中心(CDC)正被指示逐步停止所有猴子研究,涉及约200只用于艾滋病、肝炎等重大传染病研究的猕猴。如果计划落地,这将成为美国首次主动终止内部非人灵长类动物研究项目,标志着动物实验模式的历史性转折。事实上,早在今年7月,美国国立卫生研究院(NIH)便已宣布不再专门征集动物实验项目,并明确要求研究人员在设计动物研究时优先采用...
成果解读 | 新型核酸纳米载体实现对耐甲氧西林金黄色葡萄球菌的靶向及治疗
当前耐甲氧西林金黄色葡萄球菌(MRSA)因滥用抗生素引发多重耐药,其携带的mecA基因编码的 PBP2a 蛋白可逃避 β-内酰胺类抗生素杀伤,导致肺炎、败血症等致命感染频发。全球范围内,MRSA 感染不仅延长患者住院时间、增加医疗成本,现有替代抗生素疗效还因耐药菌株进化持续下降,而新型抗生素研发停滞,临床治疗陷入严峻困境。 反义寡核苷酸(ASOs)虽可靶向mecA抑制 PBP2a表达,恢复 MRSA对β-内酰胺类抗...
成果解读 | 朴衡人源化MASH模型助力解析MASH 相关肝癌发生新机制
代谢功能障碍相关脂肪性肝病(MASLD,原非酒精性脂肪肝 NAFLD)全球发病率已达 20%-25%,其严重亚型代谢功能障碍相关脂肪性肝炎(MASH)是肝细胞癌(HCC)的重要诱因,目前约占全球肝癌病例的2%,预计2030年将成为肝癌的首要病因。 与HBV/HCV相关肝癌相比,MASH 相关肝癌具有独特的分子和免疫特征,脂质过载会引发氧化应激、复制应激及核苷酸库失衡,进而导致DNA损伤和突变积累,成为关键癌前事件...
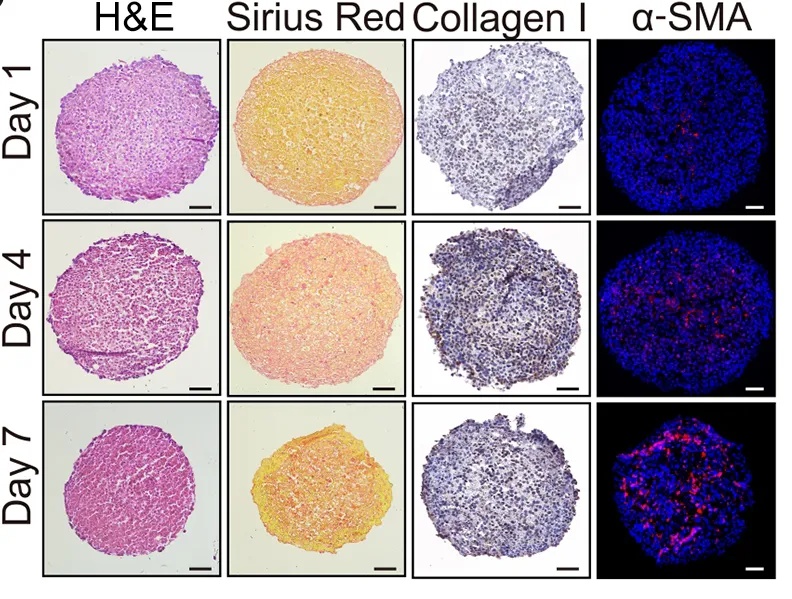
文献分享丨微流控构建的人工肝微组织用于急性肝衰竭修复
急性肝衰竭是一种危及生命的疾病,原位肝移植是最有效的治疗手段之一,但供体器官稀缺严重限制其临床应用。人工生物工程肝移植物移植成为替代方案,却面临三大核心挑战:功能性人肝细胞来源有限,人工肝移植物快速构建技术受限,移植后细胞存活能力差,难以实现长期治疗效果。 传统 3D 细胞聚集体(如细胞球状体模型)存在尺寸受限(氧和营养供应不足)、易形成坏死核心、长期培养稳定性差等问题,无法满足大规模组织工程需求。因...
产品介绍 | 朴衡博迈人源化3D肝纤维化模型
目前基于肝纤维化模型的病理及药物研究局限性较强,例如2D细胞培养过于简单,无法模拟肝非实质细胞与肝实质细胞在复杂三维空间中的相互作用。传统肝类器官3D模型通常细胞种类单一,缺乏关键免疫组分且难以主动诱导纤维化以用于疾病造模。动物模型周期长、种属差异大,其致病机制与人类临床存在差距。因此,能够整合多种细胞类型、高度模拟体内真实微环境的3D肝纤维化模型,将是精准研究疾病机制和药物筛选的理想工具。 朴衡博迈...