心血管疾病(CVD)是全球主要致死病因,心肌梗死(MI)心血管疾病占比不小且易引发心力衰竭,心力衰竭临床试验成效不佳。同时,基础研究中动物模型与人类患者脱节,且缺乏模拟人类心肌梗死急性状态的模型。药物心脏毒性也是是药物研发重点。基于此,迫切需要开发模拟心肌梗死及药物心脏毒性的人类心脏类器官模型。
纽约大学理工学院的Ying Mei教授带领团队在《nature biomedical engineering》上发表了题为《Human cardiac organoids for the modelling of myocardial infarction and drug cardiotoxicity》的论文。本文通过利用营养物质(氧气)扩散梯度和慢性肾上腺素能刺激的原理,采用了多种细胞培养、分子生物学和成像技术等方法。成功构建了能模拟心肌梗死结构和特征的心脏类器官模型。
一、人类心肌梗塞类器官的开发
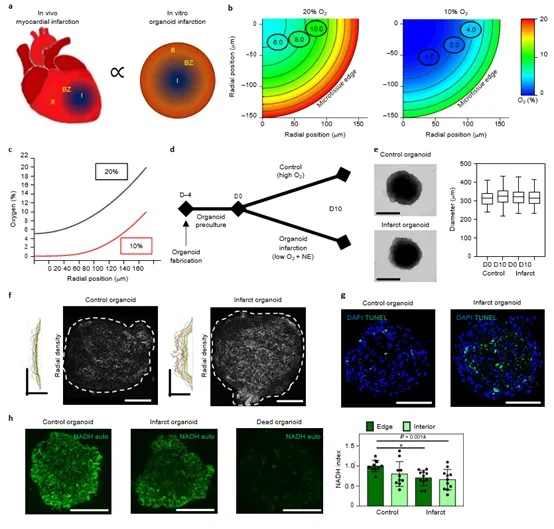
动脉阻塞限制含氧血液输送到下游心肌,导致细胞死亡因而向身体泵血能力下降从而促进神经系统分泌促甲肾上腺素去刺激心脏补偿恢复输出量。但是由于受损心脏无法完全补偿或再生,这种正反馈就会导致心脏功能障碍。基于此设计了3D类器官心肌梗死模型。有限元模拟展示了在 20% 和 10% 外部氧气条件下心脏微组织氧气扩散的量化结果,为后续实验提供理论基础。通过使用人全能干细胞诱导的心肌细胞(hiPSC-CMs)、人心室成纤维细胞、人类脂肪干细胞、人脐静脉内皮细胞构建类器官。值得注意的是,在正式构建类器官之前对hiPSC-CMs进行了为期4天的预培养。类器官直径结果表明心肌梗死在一定程度上抑制了细胞生长。活体成像、TUNEL染色和NADH荧光成像结果显示了梗死类器官内部的情况,证明了模型构建的可靠性。
二、心脏梗塞类器官的转录组荟萃分析
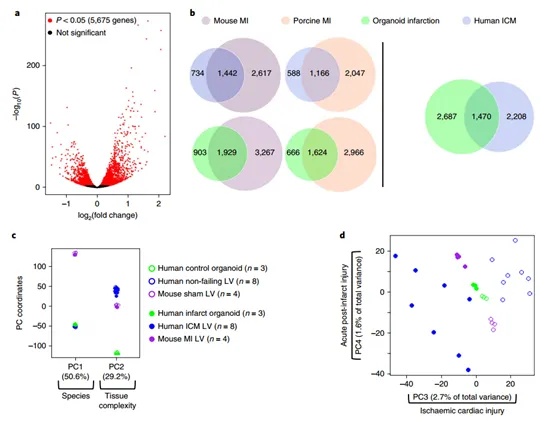
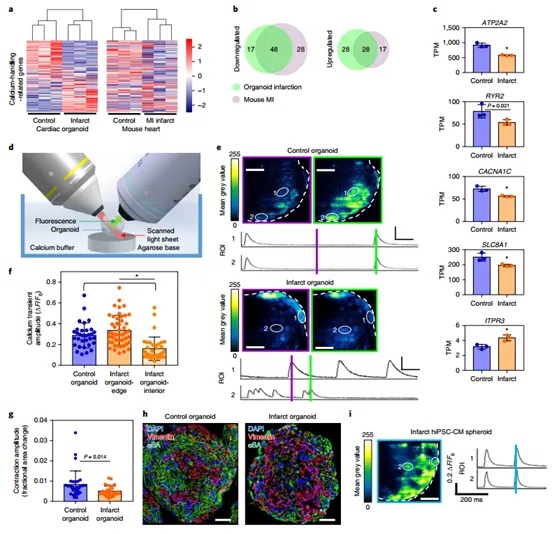
在成功构建了模拟心肌梗死的人类心脏类器官模型之后,为深入探究该模型在基因表达层面的特征及其与临床和动物研究的相关性,对心脏梗死类器官进行了转录组学分析。使用RNA-seq分析对照组和梗塞组类器官的转录组,筛选得到5675个差异基因。通过对梗塞类器官、人缺血性心肌病(ICM)与小鼠、猪的心肌梗死(MI后一周)的差异基因进行对比,得到了1000多个重叠基因,这与梗塞类器官和ICM对比结果类似。主成分结果显示梗死类器官在基因表达特征和人类样本类似,可以在一定程度上模拟人类心脏损伤,但与真实心脏组织存在差异,并且无法分析不同样本之间的差距。
三、心脏梗塞类器官的病理代谢变化
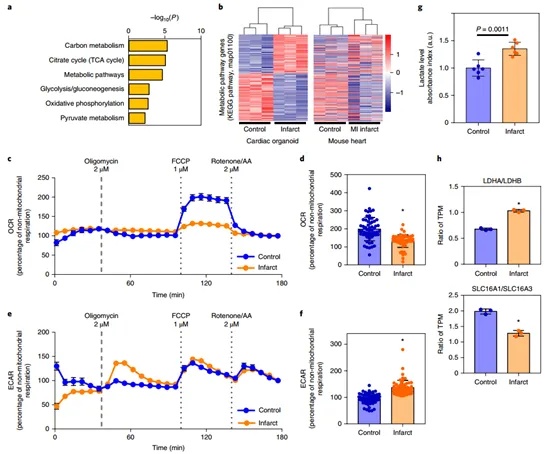
基于转录组学分析揭示的心肌梗死类器官基因表达变化,他们进一步研究了其在代谢层面的响应,以明确模型是否能模拟心肌梗死后的病理代谢转变。培育10天后的GO结果显示命中率最高的前三通路为碳代谢通路、柠檬酸(TCA)循环、糖酵解/糖异生通路。继而进行小鼠MI和梗死类器官的KEGG分析得出他们在代谢途径相关基因表达变化上呈现出相似的趋势。线粒体应激测试耗氧率(ORC)说明了梗死组类器官内部线粒体受到损伤,细胞外酸化率(ECAR)结果展示了梗死类器官内部糖酵解程度增加,进一步证明了其线粒体受到损伤。比色法测定L-乳酸、LDHA/LDHB和SLC16A1/SLC16A3结果验证了梗死类器官糖酵解的增加,这与体内心肌梗死的代谢特征相符,证明了此模型可以用来研究心肌梗死相关的代谢变化机制。
四、心脏梗塞类器官表现出病理性纤维化
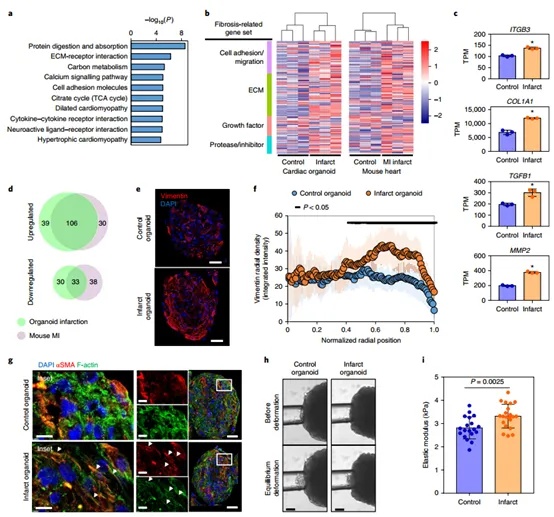
在了解心脏梗死类器官的代谢变化后,他们继续考察其在细胞和组织水平的纤维化相关特征,从而全面评估模型对心肌梗死后纤维化进程的模拟能力。GO结果显示纤维化相关通路上升。热图显示梗死类器官与小鼠 MI 后 1 周样本在纤维化相关基因表达变化趋势上高度相似。RNA-seq显示梗死类器官纤维化相关基因均上调,梗死类器官与小鼠心肌梗死样本在多个纤维化相关基因的表达趋势上呈现出一致性。Vimentin染色结果显示梗死组外围纤维化加深,细胞径向密度分布图结果验证了Vimentin结果,心肌梗塞类器官的成纤维细胞向类器官边缘迁徙。F-actin和α-SMA荧光共染色结果显示梗死类器官肌成纤维细胞的表达。细胞刚性检测结果显示梗死类器官硬度上升,更加说明了其纤维化的加剧。
五、心脏梗塞类器官中的病理钙处理
随着对心脏梗死类器官纤维化特征的研究,他们通过关注其钙处理相关的功能变化,来判断模型是否能重现心肌梗死后钙处理异常及心律失常等现象。对比梗死类器官和小鼠心肌梗死与对照组对比的RNA基因集,发现这两者基因表达变化相似。韦恩图分析显示钙处理相关基因表达上的相似性。梗死类器官钙处理相关基因下调说明细胞受到了一定损伤。钙释放基因上调可能是因为在心肌梗死早期,一定程度的细胞内钙释放增加有助于激活某些细胞保护机制或参与细胞对损伤的应激反应。为了观察钙动态变化,他们开发了一个双光子显微镜。结果显示与对照组相比,梗死组内部钙信号较弱,与外界不同步且存在心律不齐的现象。收缩幅度分析显示梗死类器官的收缩功能受到影响,这个结果与钙处理异常密切相关,因为钙信号在心肌细胞收缩过程中起着关键的调节作用。αSA和Vimentin荧光共染色结果显示正常类器官心肌细胞紧密结合,梗死类器官心肌细胞被成纤维细胞隔开,使其链接被破坏,影响细胞信号传递和收缩。为了证明成纤维细胞在钙处理中的作用,他们用仅含hiPSC-CMs的细胞球体在梗死类器官培养下的钙信号情况,结果显示并未存在心率失常现象,这证明成纤维细胞在钙处理异常中的关键作用。
六、组织水平的心力衰竭药物测试
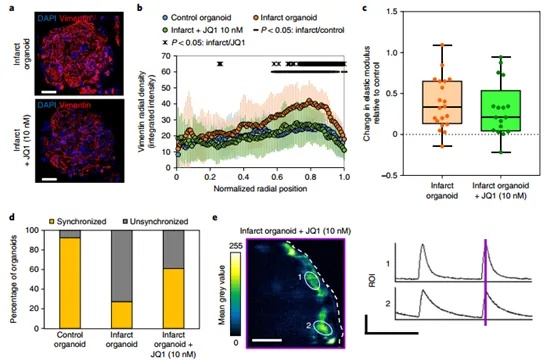
在明确心脏梗死类器官的钙处理异常及心律失常特征后,他们就将模型应用于药物测试,首先他们探索抗纤维化药物溴结构域抑制剂(JQ1) 对梗死类器官的影响,以评估这个模型在药物研发中的潜力。添加了JQ1之后,Vimentin染色结果显示成纤维细胞被抑制,细胞径向分布结果证明了染色的结果。弹性模量分析显示JQ1对类器官硬度影响较小。自发跳动分析结果也证实了JQ1对纤维化是存在改善作用的。钙成像说明了JQ1的对钙处理也是有改善作用的。从多维度验证JQ1的抗纤维化作用。
七、组织水平药物引起的心脏毒性加剧
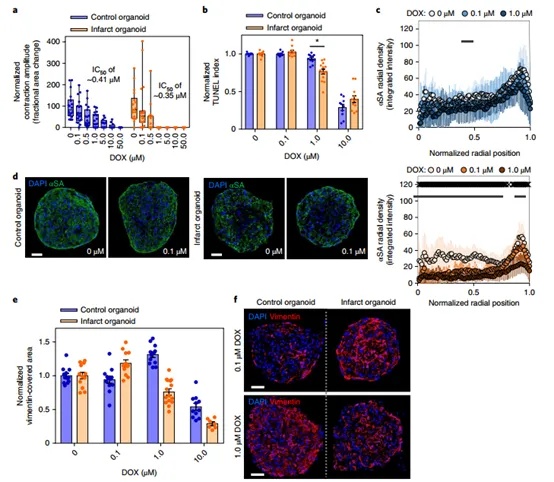
在利用模型进行抗纤维化药物测试后,为了进一步研究它在检测药物诱导的心脏毒性的能力,他以阿霉素(DOX)为例,观察模型对药物加剧心脏毒性的反应。梗死类器官在低浓度DOX(1μM)时,收缩幅度显著降低,说明预先存在的心脏损伤加剧了 DOX 的心脏毒性,影响了类器官的收缩功能。TUNEL染色补充说明了其在1μM的DOX时,凋亡显著增加。并且随着 DOX 剂量增加,梗死组类器官中肌节结构的紊乱程度比对照组更严重,尤其是内部区域。0.1 µM DOX 处理后,梗死组类器官内部的心肌细胞相较于对照组,荧光强度变低分布变散,纤维化覆盖面积增加,而对照组在1μM时纤维化程度才有明显增加,这表明 DOX 对预先存在损伤的梗死组影响更早且更显著。Vimentin直观地显示了对照组和梗死组纤维化的情况。上述结果说明,该模型可用于检测药物诱导的心脏毒性加剧情况,为研究药物在心肌梗死患者中的心脏毒性提供了重要模型。
八、创新点
1、利用氧扩散梯度和去甲肾上腺素刺激,构建了一种模拟心肌梗死后心脏组织的人类心脏类器官模型。
2、开发了双光子成像仪器动态显示钙处理。