Unit 615, No. 2, Lane 388, Kangan Road, Pudong New Area, Shanghai, China
News Center
文献分享 | 新突破:类器官模型揭示新冠病毒引发糖尿病β细胞焦亡机制
背景:
冠状病毒疾病19(COVID-19)与糖尿病之间的强烈联系现在得到了承认。自疫情开始以来,已有新发糖尿病的报告。此外,观察到1型糖尿病(T1D)的发病率有所上升。美国疾控中心的一项研究发现,与未感染COVID-19的人相比,年龄在18岁以下的COVID-19患者更有可能被诊断出患有糖尿病。有研究报告称,在疫情开始后,1型糖尿病(T1D)和2型糖尿病(T2D)的发病率有所上升,超过了疫情前时期。
除了严重急性呼吸综合征冠状病毒(SARS-CoV-2)外,许多研究表明病毒感染与T1D之间存在相关性,包括肠道病毒,如柯萨奇病毒B、以及轮状病毒、腮腺炎病毒、和巨细胞病毒。柯萨奇病毒B4(CVB4)是一种从新诊断的T1D患者中分离出来的正义单链RNA病毒,可在体外感染并诱导人类胰岛细胞的破坏然而,目前还缺乏人体模型来研究免疫介导的宿主损伤。

2024年9月3日,威尔康奈尔医学院陈水冰教授等人在Cell Stem Cell期刊发表了题为:Human vascularized macrophage-islet organoids to model immune-mediated pancreaticβcell pyroptosis upon viral infection的研究论文。
该研究运用空间多组学分析技术全面分析了COVID-19患者的胰腺病理样本,发现COVID-19样本中存在促炎性巨噬细胞的积累.单细胞RNA测序(scRNA-seq)分析证实,暴露于新冠病毒(SARS-CoV-2)或柯萨奇病毒B4型(CVB4)的人类胰岛β细胞中存在促炎巨噬细胞的激活,并显示出细胞焦亡通路的富集。
接下来,研究团队开发了一种含有人多能干细胞(hPSC)来源的内分泌细胞、巨噬细胞和内皮细胞的血管化巨噬细胞-胰岛(VMI)类器官模型,发现促炎性巨噬细胞通过分泌IL-1β并通过TNFSF12-TNFRSF12A通路与β细胞相互作用,从而导致β细胞发生细胞焦亡
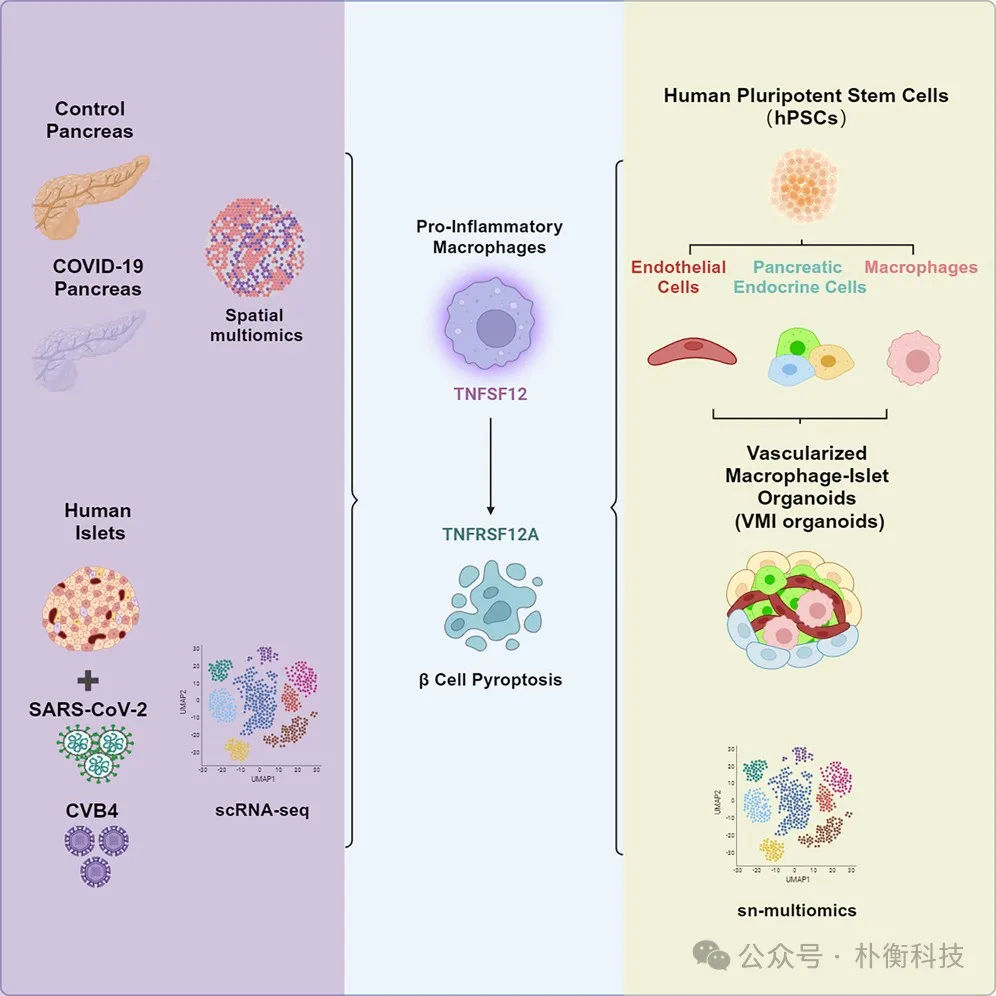
通过分析人类血管化巨噬细胞-胰岛类器官在病毒感染后的单细胞RNA测序数据,作者发现SARS-CoV-2或CVB4病毒感染可以诱导胰岛β细胞发生焦亡,这是一种程序性细胞死亡。研究揭示了病毒感染后,胰岛中促炎性巨噬细胞和单核细胞的富集,并观察到与细胞焦亡相关的基因表达上调。此外,研究还发现在病毒感染的胰岛β细胞中,与自身免疫相关的基因表达增加。这些发现为理解病毒感染如何影响胰岛β细胞,以及可能诱发自身免疫反应的机制提供了新的视角,为糖尿病和相关代谢疾病的研究和治疗提供了潜在的新靶点。
