Unit 615, No. 2, Lane 388, Kangan Road, Pudong New Area, Shanghai, China
News Center
文献解读 | Nature 重大突破!构建具有组织驻留免疫细胞的人肠道类器官
肠道粘膜免疫系统-人体最大的免疫细胞库-对维持肠道稳态和预防肠道疾病等方面发挥重要作用,但目前的肠道类器官只能模拟上皮细胞类型的分化和功能,在捕捉肠道(病理)生理学的关键方面存在不足,原因是缺乏特定组织的免疫细胞群。近日,瑞士人类生物学研究所(IHB)发表最新研究,成功构建出人类肠道免疫类器官(IIOs)。该模型包含人体组织样本中的组织驻留和自体免疫细胞群,基于该模型文章探讨了自体组织驻留记忆T (TRM)细胞与上皮细胞之间的相互作用以及它们如何通过影响细胞运动和粘附的转录组程序来协调这些相互作用,并利用IIOs来重现和研究药物诱导的肠道炎症。

首先作者采用了一种无酶、基于支架的方法分离出大量的肠道免疫细胞,相比于酶解方法能释放出更多的免疫细胞,同时保持了类似的免疫细胞类型比例。分离出的免疫细胞大多数为组织驻留记忆T细胞,并保持了肠道相关的TRM细胞标记,与血液来源的PBMC有所差异。然后将收集的免疫细胞与肠道类器官进行共培养,TRM细胞 在没有刺激的情况下能够渗透到类器官中,并整合到肠道上皮屏障内,类似于肠道上皮内淋巴细胞(IELs)的行为,而与肠道类器官共培养的PBMC 难以整合到上皮细胞,只存在于基质中。
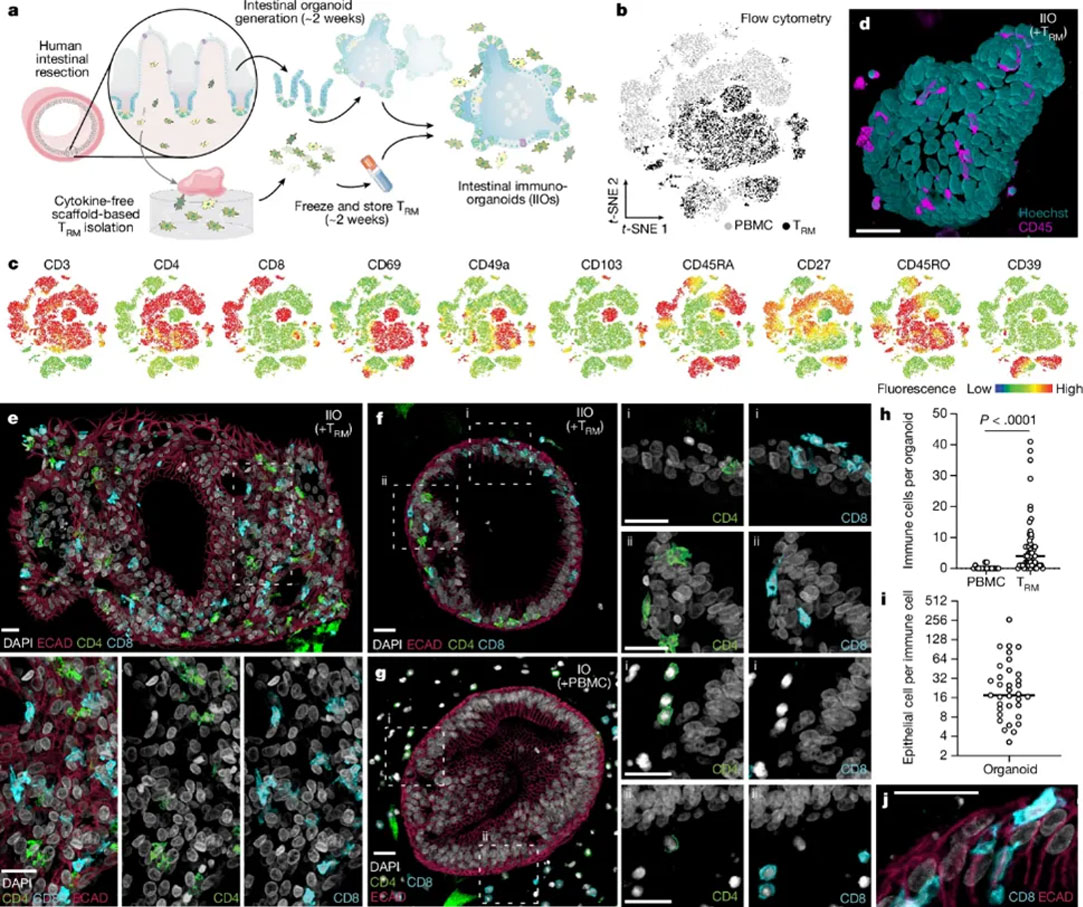
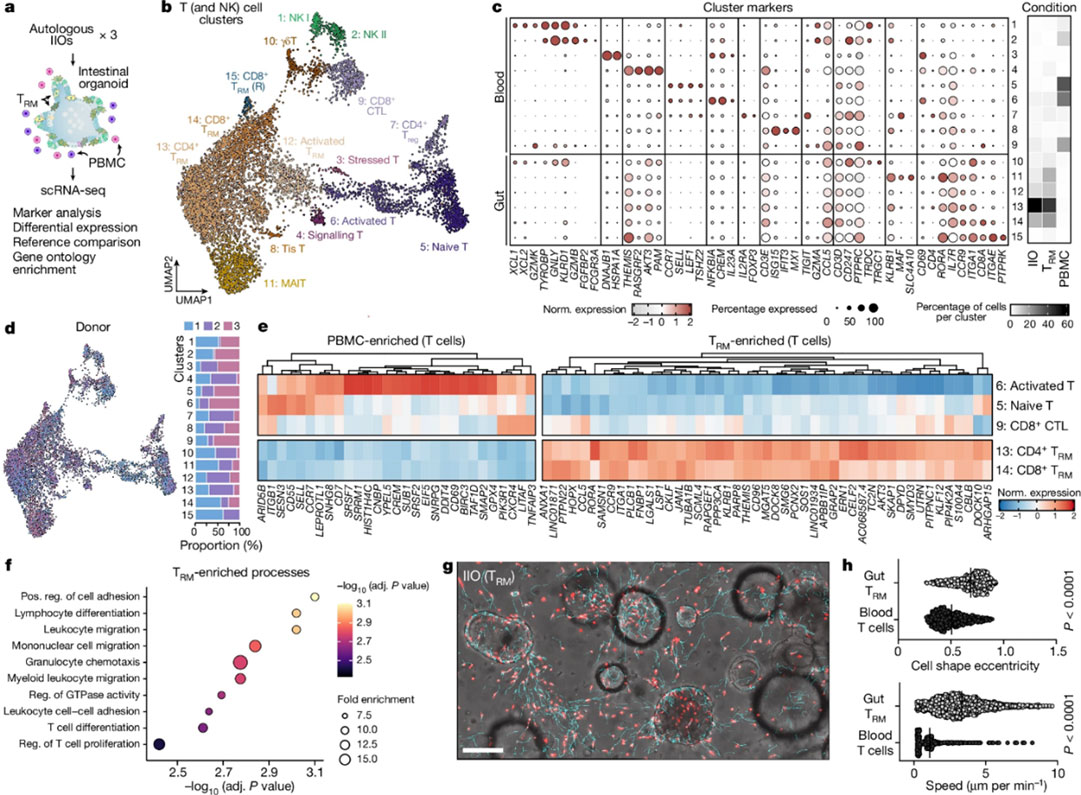
为了探究TRM细胞和PBMCs在体外与肠道上皮细胞整合的差异,作者用单细胞RNA测序(scRNA-seq)来分析来自三个不同小肠样本的IIOs。结果发现IIOs的TRM细胞与肠道内淋巴细胞具有相似的转录组特征,包括缺乏淋巴结归巢受体、高表达肠道归巢和整合因子以及缺乏细胞毒性颗粒。与PBMCs相比,TRM细胞中与免疫细胞趋化和迁移相关的转录组程序富集,这可能解释了它们在上皮内整合的倾向。
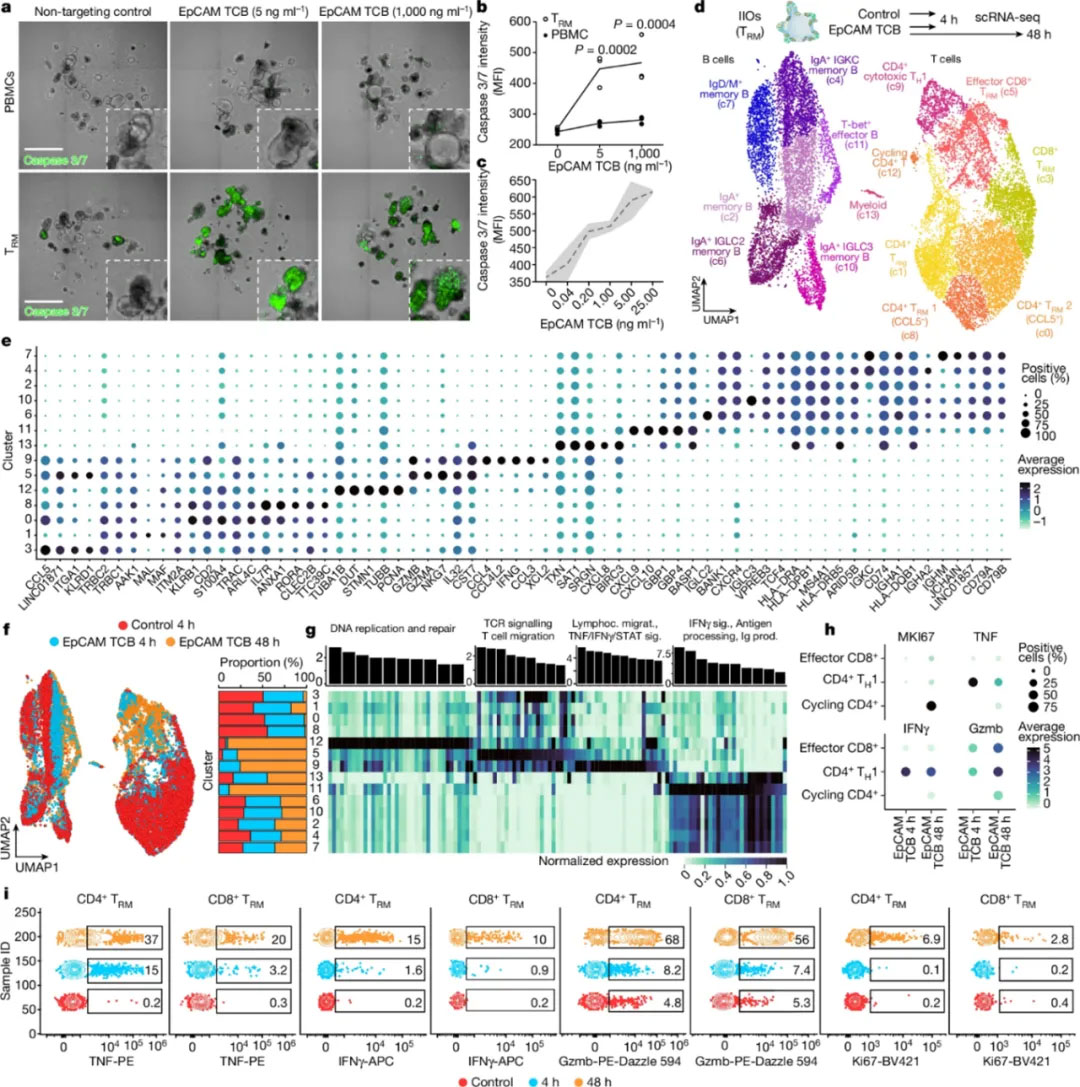
接着探究TRM细胞和PBMCs转录组和迁移行为的差异是否会转化为效应功能的差异,作者用靶向上皮细胞的双特异性T细胞结合分子(TCB),观测IIOs是否能重现与癌症免疫治疗相关的临床毒性。结果发现,TRM以TCB剂量依赖性方式靶向上皮细胞,并诱导上皮细胞凋亡。通过转录组学动态分析TRM细胞靶向治疗引起细胞毒性效应的机制,研究结果表明,炎症与CD8+ T细胞的激活有关,这些细胞逐渐获得了上皮内和细胞毒性特征。作者发现IIOs细胞异质性动态与患者体内药物诱导得结肠炎的动态相似,包括细胞毒性CD8+T细胞得出现和调节性T细胞的减少。这些相似性表明,IIOs可以用于在体外环境中重现和研究肠道炎症。
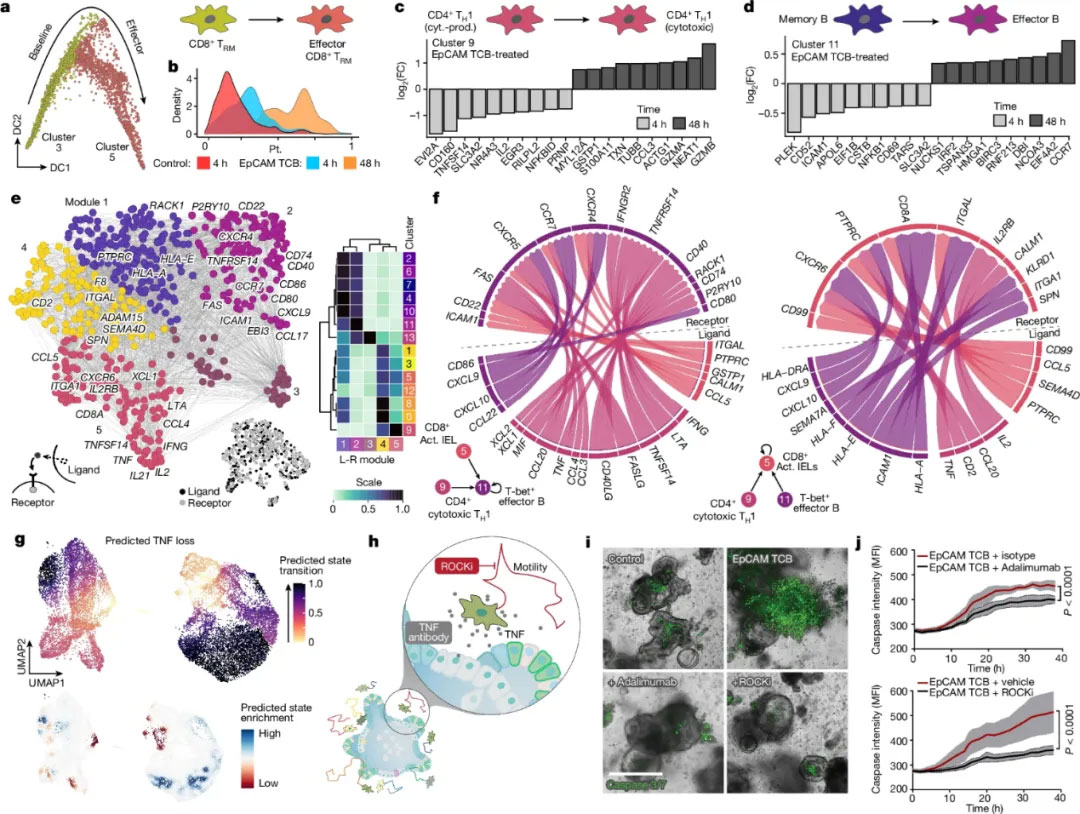
作者进一步分析这一动态过程中如何通过细胞间信号传导激活表型,发现TCB处理后CD4+辅助性T细胞1(TH1)群体会分泌多种信号因子 指导B细胞(c11)和CD8 T细胞(c5)发挥作用。此外作者用TNF阻断抗体和Rho信号通路抑制剂可以有效抑制TCB诱导的肠道炎症,这为减轻免疫治疗相关肠道炎症提供新靶点。
总之,这篇文章提供了关于如何构建和利用人类肠道免疫类器官来研究免疫细胞与上皮细胞相互作用的详细信息,以及如何通过这些模型来研究和治疗相关的疾病,为未来的免疫学研究和治疗策略的开发提供了新的方向。
- Previous article:文献分享 | 利用人类多能干细胞模拟人类骨骼发育
- next:文献分享 | 新突破:类器官模型揭示新冠病毒引发糖尿病β细胞焦亡机制
