Unit 615, No. 2, Lane 388, Kangan Road, Pudong New Area, Shanghai, China
News Center
NAC-Organ技术应用于NASH研究:新一代3D模型的构建与药物开发前景
非酒精性脂肪性肝炎(NASH)是一种进行性和严重的肝脏疾病,其特征是脂质积聚、炎症和纤维化。进而发展成肝硬化、肝癌和肝衰竭,虽然大量治疗NASH候选药物已经进入临床测试,但由于疗效有限,至今未有获得批准治疗NASH的药物。药物研发会经历从药物探索、药学研究、临床前研究到临床研究再到审批与上市的过程,而临床的转化效率不到10%,临床前使用的研究模型与临床相关度偏低是重要原因之一。
NASH动物模型存在局限性
当我们探索治疗NASH的药物时,动物模型在研发过程中扮演着不可或缺的角色。这些模型通过模拟人体内的生理和病理过程,为科学家提供了研究新疗法的平台。然而,正如所有研究工具一样,动物模型也存在一些局限性。
目前常用的NASH动物模型有以下几类:1) 高脂饮食诱导的NASH模型;2)营养素缺乏饮食诱导的NASH模型;3)化学毒素诱导的NASH模型。4)基于基因编辑小鼠构建的NASH模型。
-
高脂饮食诱导的NASH模型
代谢紊乱疾病患病率的增高很大程度上源自人们的饮食结构的改变。采用西方饮食饲料的喂养充分模拟代谢疾病人群高热量,高糖分以及高胆固醇的饮食特点,诱导后产生肥胖、高血糖、高血脂等代谢紊乱特征,同时表现出一定程度的脂肪变性、炎症、气球样变或纤维化表型,但其造模周期很长,需要20~30+周,一定程度上限制了药效评价实验推进的速度。
-
营养素缺乏饮食诱导的NASH模型
除了高热量饮食外,利用缺乏营养素(如蛋氨酸、胆碱缺乏)的特殊饲料喂养也能够获得具有脂肪肝病表征的小鼠模型。蛋氨酸+胆碱缺乏饲料(MCD)饲喂3周左右可见明显的脂肪性肝炎病变, 8周后可见肝纤维化。这类小鼠模型虽能够呈现肝脏的病理表现,但小鼠无肥胖、高血糖及高血脂表型。因此,此类模型也不能很好复刻人类NASH病症。
-
化学毒素诱导的NASH模型
为了缩短饮食诱导造模的周期,研究者们在高脂饲料饲喂前引入化学毒素(链脲佐菌素,STZ)诱导。这种造模方式造模周期较短,也能够获得较全面的脂肪肝病理表型,但不同批次之间的STZ毒素存在差异,且实验条件、人为操作等差异都会对模型的效果产生一定影响。这种方法诱导的NASH模型均没有肥胖、胰岛素抵抗的表征。在更强调全身代谢紊乱综合征与肝脏病理变化发展关系的今天,显然这一类模型难以匹配人类脂肪肝病的研究。
-
高脂饮食诱导的NASH模型
BKS-db是一种经典II型糖尿病模型,它具有严重的肥胖表型,同时具有高血糖症、高血脂症和胰岛素抵抗等代谢紊乱特征,并且随着周龄增加,在大周龄BKS-db(约16周)中可以观察到一定程度的脂肪肝表型。该模型构建周期短,仅喂养4周小鼠便出现了更高的体重、血糖和血脂水平,同时具有严重的肝脏损伤以及典型的肝脏NASH样病变。但基于瘦素信号通路受损,该模型纤维化表型很弱,并且BKS-DB小鼠并发症较严重。
在针对NASH药物研发的过程中,NASH的动物模型为阐明该疾病的发病机制和开发新的治疗方法提供了重要信息,有着不可否认的价值。但同时必须认识到,由于人和动物代谢酶的不同,模式动物建构的NASH模型无法完全模拟人类的生理情况。此外,大多数的NASH动物模型都需要相当长的时间才能有相应的症状出现。不仅如此,NASH疾病的极端多样性意味着NASH的动物模型本身也是可变的,而且组织病理学特征也很难出现稳定的状态。
体外3D培养技术
2021年,美国参、众两院相继通过FDA相关修订法案,首次将体外3D培养作为独立的药物非临床实验评估体系纳入法案。FDA认为,体外3D肝模型为系统性替代模式动物提供了可行的方案,并且可以用于药物安全性和毒性的评估。3D培养技术是能模拟人体内功能的体外技术,可为药物开发和组织工程等应用提供快速且经济高效的模型。目前传统类器官多采用多能干细胞进行分化,其构建3D模型比较复杂,生产周期长,同时还需要较多的生长因子和基质胶的参与,生产成本较高。另外,构建复杂模型时易受限于细胞类型,如果采用支架,将人原代细胞植入其中,从单个细胞到3D微组织,最少也需7天才可用于筛药。
基于NAC-Organ技术构建的NASH模型
NAC-Organ是朴衡基于细胞膜工程技术理念研发的新型 3D 培养模型构建技术。为解决现有3D培养技术存在的问题,提供更适合药物筛选大规模应用的3D模型。NAC-Organ技术兼具3D细胞微球重复性好、均一性高,和类器官模拟目标器官生理、病理结构的能力,并具有构建速度快、操作简单的特点,可以为药物研发提供标准化、高通量的筛选、验证工具。
利用NAC-Organ技术构建的3D肝脏模型(NAC-Liver),将原代肝细胞、原代肝窦内皮细胞、原代肝星状细胞和原代Kuffer细胞在24小时内进行快速组装,减少原代肝细胞在体外培养时间。NAC-Liver可在体外稳定维持超过30天,能够长时间维持药物代谢酶的活性,可以用于药物肝毒性的高通量检测,大幅降低药物研发的成本。
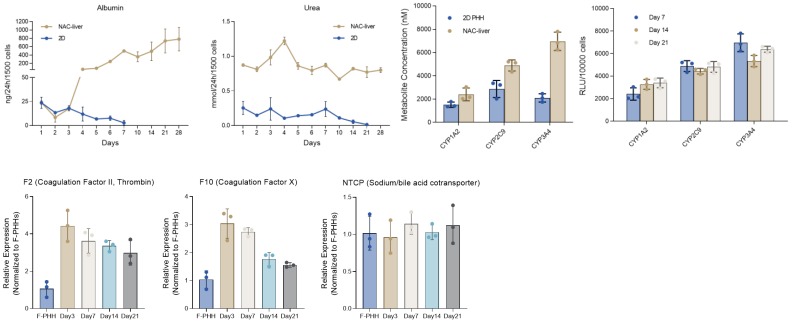
NAC-Liver比2D培养肝细胞能够更好的维持肝脏生理功能
针对NASH新药研发火热且缺乏适当的研究模型这一巨大的市场需求,我们利用NAC-Organ的技术特点,重点研发了第二代体外3D NASH模型。相较于第一代体外3D NASH模型,第二代3D NASH模型不但可以模拟NASH疾病的脂肪病变、炎症反应、纤维化病变,还首次在NASH体外模型中实现了成纤维细胞的病理分布,直接模拟体内假小叶结构,可以反映纤维化病变对药物递送及药效的影响,能更准确地预测NASH药物的体内药效,可应用于纤维化药物研发新靶点筛选。
朴衡科技的NAC-Organ肝纤维化模型助力科学研究并得到了实质性的成果。研究表明,该模型中过表达TrkB能够有效抑制肝星状细胞的激活和增殖,从而实现了对纤维化的缓解。这一发现不仅在体外模型中得到验证,还在动物体内模型中得到了证实,相关结果已发表在《Hepatology》[1]。为TrkB成为治疗肝纤维化的潜在靶点提供了有力的科学依据。

NASH模型模拟NASH疾病的脂肪病变、炎症反应、纤维化病变
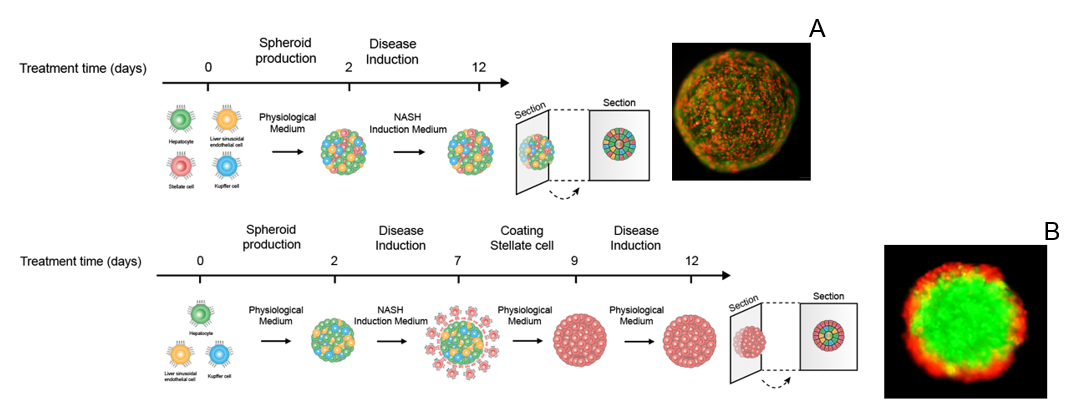
NAC-Organ第二代NASH模型与现有NASH模型比较
A:第一代NASH模型中成纤维细胞(红色)随机分布;
B:第二代NASH模型能够模拟成纤维细胞(红色)的病理分布,形成类似假小叶的结构,影响肝细胞对药物的养分、药物的吸收。
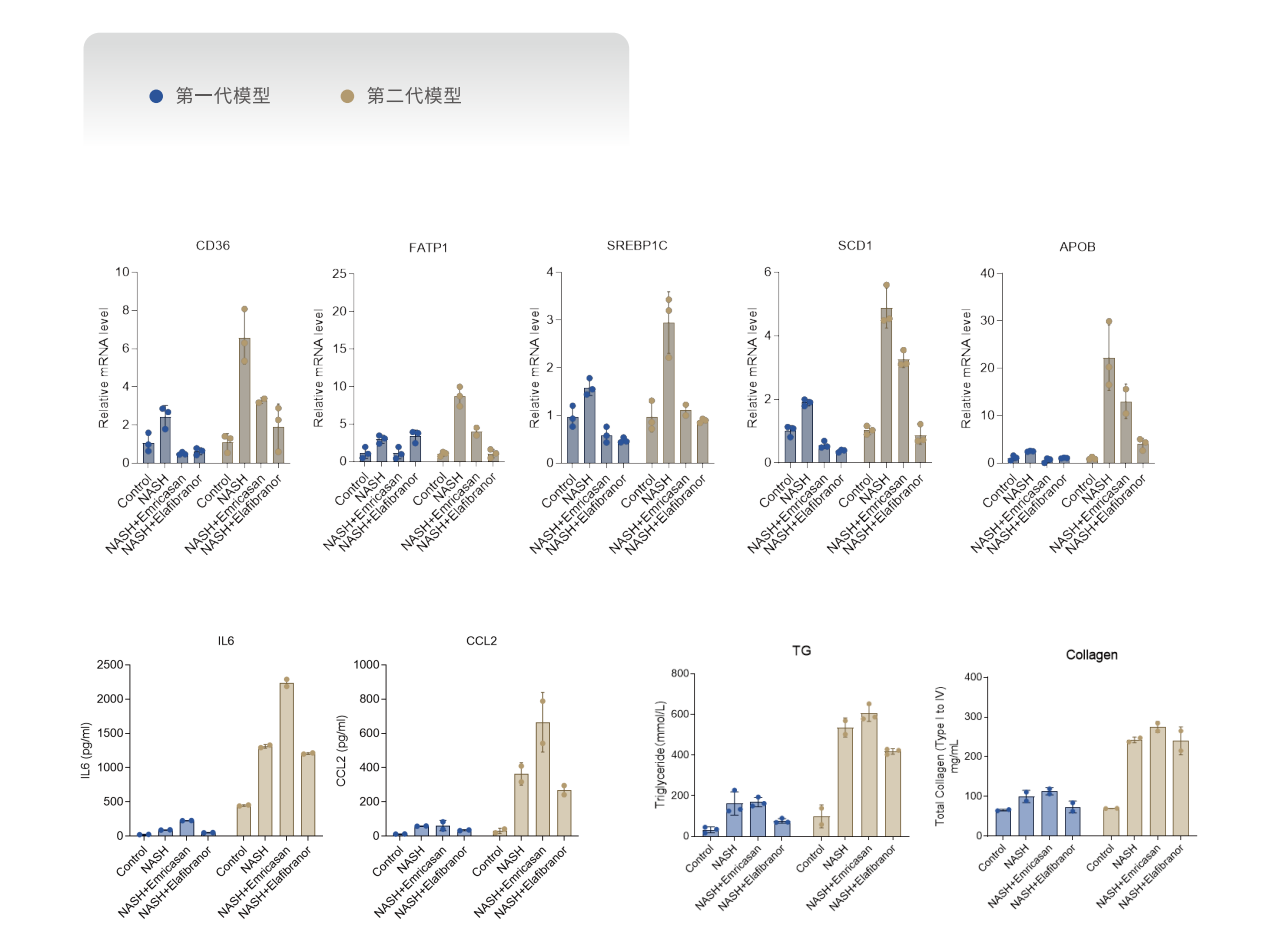
第二代NASH模型用于药物筛选能够好的预测体内药效
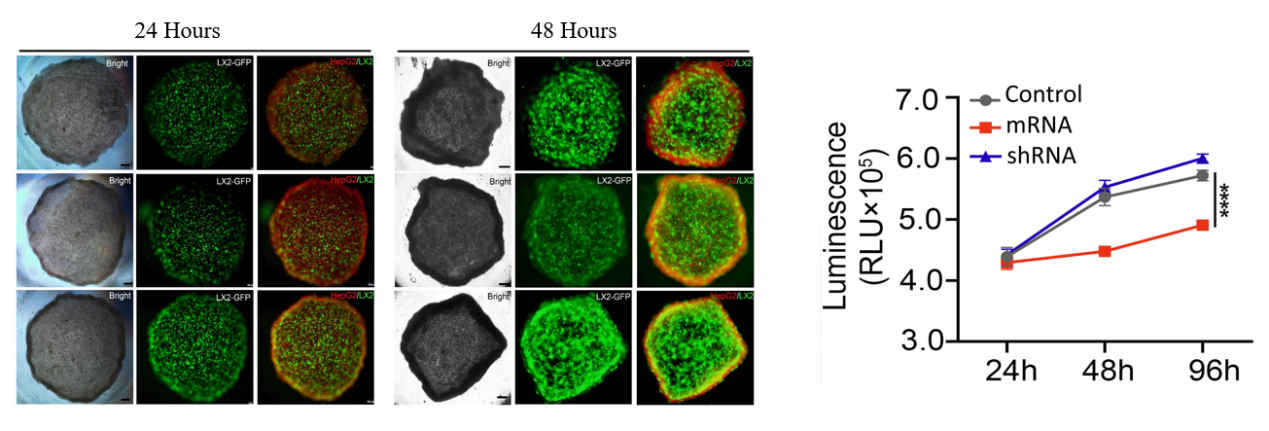
NAC-Organ模型筛选用于NASH、纤维化药物研发的新靶点
朴衡服务清单

- Previous article:强强联合,共创共赢 | 朴衡科技与凯斯艾生物签署战略合作协议
- next:看得见的浸润 | 朴衡科技助力鲲石生物发布CAR-M体外3D评估模型成果
