Unit 615, No. 2, Lane 388, Kangan Road, Pudong New Area, Shanghai, China
News Center
文献分享|研究揭示 ATF4 通过增强子程序调控肝星状细胞活化与 ECM 沉积
update time:2026-02-11 11:22:00Number of clicks:311
肝纤维化(Liver Fibrosis)作为非酒精性脂肪肝(NAFLD)、酒精性肝病、病毒性肝炎等多种肝损伤的共同病理结局,表现为肝内细胞外基质(ECM)过度沉积,并呈进行性发展,若不及时干预,将进一步进展为不可逆的肝硬化甚至原发性肝癌(HCC)。肝脏的天然修复机制中,肝星状细胞(HSCs)是核心的纤维化效应细胞。正常状态下 HSCs 呈静息态,储存脂质。当肝组织受损时,HSCs 被激活并转分化为肌成纤维细胞样细胞,大量合成并分泌胶原等 ECM 成分。然而HSCs 活化机制尚未探明,且肝纤维化作为疾病可逆阶段,临床缺乏直接靶向纤维化进程的有效疗法,仅能通过消除肝损伤病因间接延缓病情,以上现状使得肝纤维化的精准治疗成为临床重大挑战。
尽管临床上针对肝纤维化的基础研究已探索多种潜在通路,但此前研究多聚焦于全身信号调控,未精准定位关键效应细胞(如 HSCs)的特异性分子。部分研究提及转录因子 ATF4 与肝纤维化的关联,却因未实现 HSCs 特异性干预,且 ATF4 的经典功能被限定于内质网应激调控,其在非应激纤维化场景下的作用机制仍未被揭示。
近日,浙江大学医学院转化医学研究院的冯宇雄研究员团队联合美国德克萨斯大学的李文博教授以及西湖大学的尤佳副研究员在Nature Communications 发表题为“Alleviation of liver fibrosis by inhibiting a non-canonical ATF4-regulated enhancer program in hepatic stellate cells”的研究论文。该团队首次发现 ATF4 在 HSCs 中具有非经典功能 —— 在 TGFβ 等纤维化信号调控下,通过结合EMT相关基因的增强子,驱动 HSCs 活化与 ECM 沉积。通过 HSCs 特异性 ATF4 敲除小鼠与小分子药物干预,证实靶向 ATF4 可有效缓解多种模型的肝纤维化,且人类肝硬化样本中 HSCs 的 ATF4 表达与疾病严重程度(Fib-4 评分)显著正相关。不仅阐明了 ATF4 调控肝纤维化的全新机制,更为临床肝纤维化的精准靶向治疗提供了新靶点与潜在药物。以下我们为您带来该研究成果的详细解读:
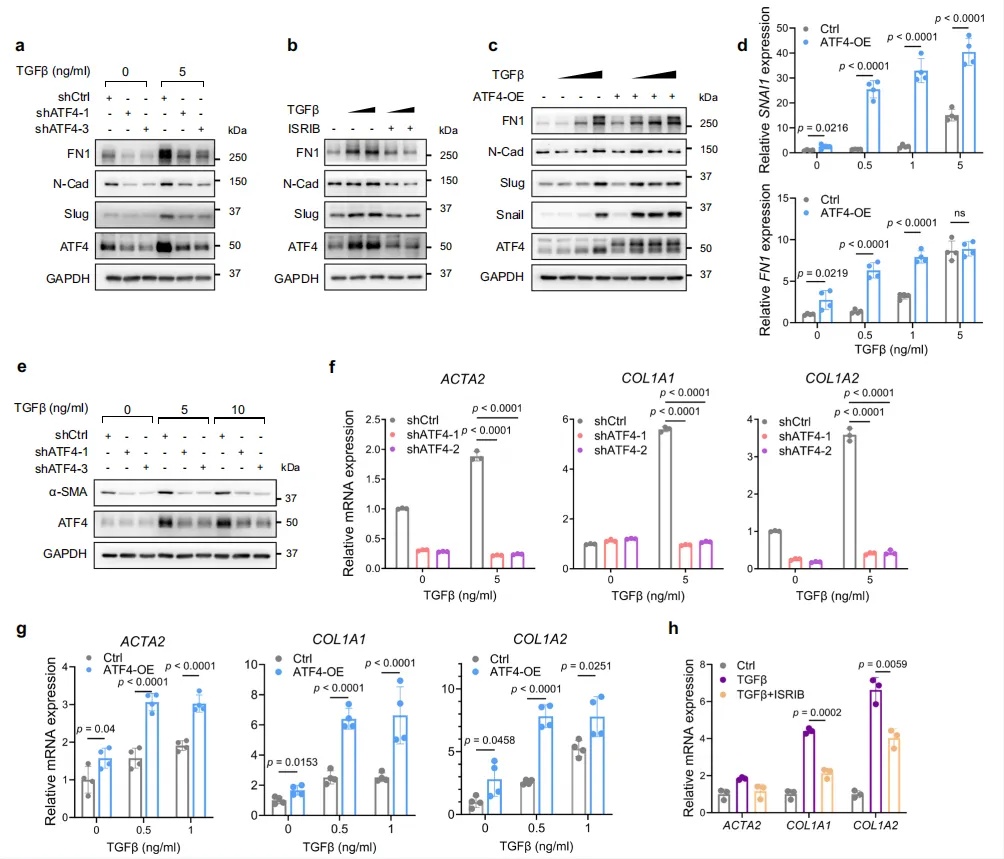
1. ATF4 在 HSCs 活化过程中的作用及调控机制初探
研究人员以 LX2 人 HSCs为核心模型,通过 ATF4 敲低(shATF4)、过表达(ATF4-OE)及小分子药物 ISRIB(抑制 ATF4 翻译)干预,结合 TGFβ/PDGF-BB(两种经典 HSCs 活化信号)处理,验证 ATF4 对 HSCs 活化作用。Western blot 与 qPCR 结果显示TGFβ 诱导的间充质标志物FN1、N-cadherin与纤维化标志物α-SMA、COL1A1、COL1A2表达均依赖 ATF4,且 ATF4 过表达可放大TGFβ 效应。ISRIB 可显著抑制 TGFβ/PDGF-BB 诱导的 HSCs 活化,且该效应能被 ATF4 过表达挽救,证明 ISRIB 的抗纤维化作用依赖 ATF4。此外,对比肝细胞(AML12),ATF4 对 ECM 基因的调控在 HSCs中更显著,体现出明确的细胞特异性。该实验首次在 HSCs 中证实 ATF4 的促活化作用(图1)。
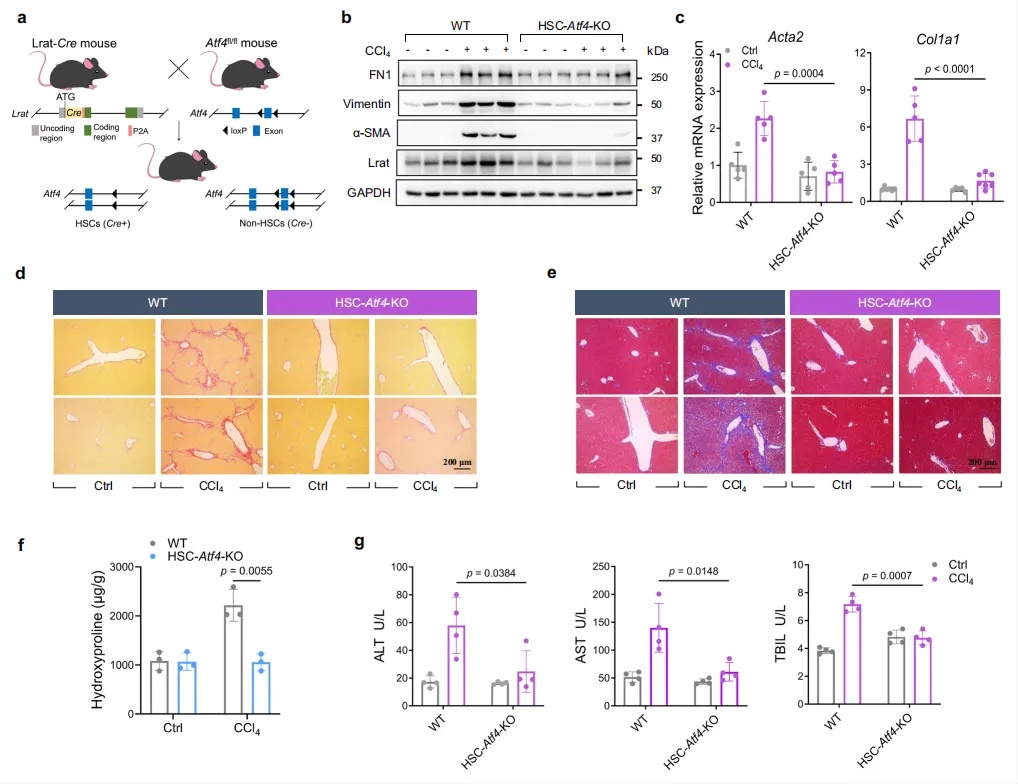
2. HSCs 特异性敲除 ATF4 对小鼠肝纤维化的体内干预效果
为验证 ATF4 在体内肝纤维化进程中的必要性,研究人员构建了 HSCs 特异性 ATF4 敲除小鼠,并通过 CCl₄诱导肝纤维化模型进行验证。与野生型小鼠相比,HSCs-ATF4-KO 小鼠肝组织中,Western blot 与 qPCR 结果显示 CCl₄诱导的间充质标志物FN1、VIM与纤维化标志物α-SMA、COL1A1、COL1A2表达显著降低。天狼星红染色和 Masson 三色染色显示胶原沉积明显减少,羟基脯氨酸定量进一步证实胶原水平下降。同时血清肝功能指标检测显示肝损伤程度减轻。该实验通过细胞特异性敲除模型,在体内证实HSCs 中的 ATF4是肝纤维化的必需因子(图2)。
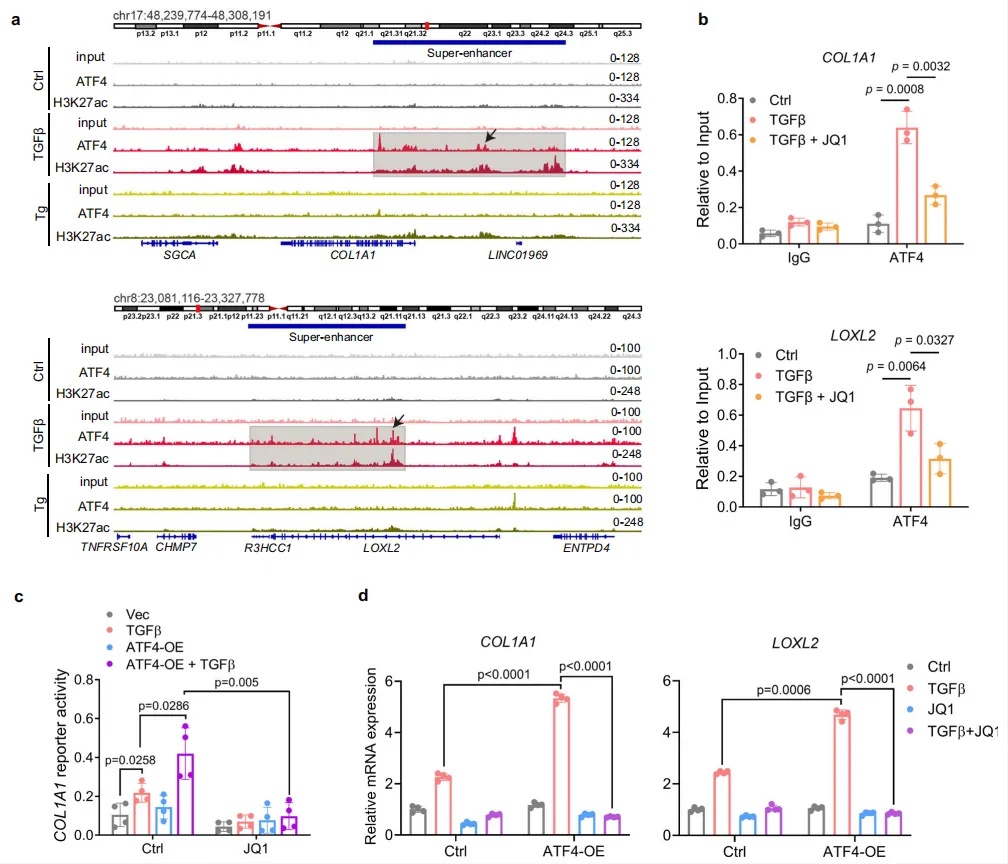
3. ATF4 通过增强子调控 COL1A1/LOXL2 等纤维化靶基因转录
研究人员通过 ChIP-qPCR、荧光素酶报告基因实验及 JQ1(增强子抑制剂)干预,验证ATF4 - 增强子 - 靶基因的调控关系。ChIP-seq 可视化显示,TGFβ 处理下 ATF4 可结合 COL1A1/LOXL2 的增强子区域,且这些区域伴随 H3K27ac 富集(COL1A1/LOXL2 为超增强子,CDH2 为典型增强子)。ChIP-qPCR 证实,TGFβ 可增强 ATF4 与靶基因增强子的结合,而 JQ1(抑制 BRD4、阻断增强子活性)可显著抑制该结合;荧光素酶报告基因实验显示,含 COL1A1 增强子的报告基因活性依赖 TGFβ 与 ATF4,JQ1 可完全阻断该活性。明确了 ATF4 通过结合增强子直接调控纤维化靶基因(图3)。
朴衡博迈开发的人源化3D肝纤维化模型(NF-HS-2-01)采用成熟的人原代肝实质细胞、肝窦内皮细胞、肝星状细胞与库普弗细胞构建。该模型克服了传统肝类器官成熟度不足与细胞类型单一的缺陷,相比普通2D细胞培养,能更有效地重现肝脏生理微环境,且无种属差异。其细胞活性及代谢能力显著优于传统2D系统,加之建模周期短,可快速应用于高通量药物筛选及靶点功能验证。作为研究慢性肝病发病机制和进行高通量药物筛选的理想工具,朴衡博迈构建的人源化 3D 肝脏模型已成功助力多项研究成果发表于 Hepatology、Gut、Cellular & Molecular Immunology、Cancer Communications 等国际高水平期刊。
尽管临床上针对肝纤维化的基础研究已探索多种潜在通路,但此前研究多聚焦于全身信号调控,未精准定位关键效应细胞(如 HSCs)的特异性分子。部分研究提及转录因子 ATF4 与肝纤维化的关联,却因未实现 HSCs 特异性干预,且 ATF4 的经典功能被限定于内质网应激调控,其在非应激纤维化场景下的作用机制仍未被揭示。
近日,浙江大学医学院转化医学研究院的冯宇雄研究员团队联合美国德克萨斯大学的李文博教授以及西湖大学的尤佳副研究员在Nature Communications 发表题为“Alleviation of liver fibrosis by inhibiting a non-canonical ATF4-regulated enhancer program in hepatic stellate cells”的研究论文。该团队首次发现 ATF4 在 HSCs 中具有非经典功能 —— 在 TGFβ 等纤维化信号调控下,通过结合EMT相关基因的增强子,驱动 HSCs 活化与 ECM 沉积。通过 HSCs 特异性 ATF4 敲除小鼠与小分子药物干预,证实靶向 ATF4 可有效缓解多种模型的肝纤维化,且人类肝硬化样本中 HSCs 的 ATF4 表达与疾病严重程度(Fib-4 评分)显著正相关。不仅阐明了 ATF4 调控肝纤维化的全新机制,更为临床肝纤维化的精准靶向治疗提供了新靶点与潜在药物。以下我们为您带来该研究成果的详细解读:

Nat Commun. 2025 Jan 9;16(1):524.
doi: 10.1038/s41467-024-55738-1.
原文链接:https://www.nature.com/articles/s41467-024-55738-1
1. ATF4 在 HSCs 活化过程中的作用及调控机制初探
研究人员以 LX2 人 HSCs为核心模型,通过 ATF4 敲低(shATF4)、过表达(ATF4-OE)及小分子药物 ISRIB(抑制 ATF4 翻译)干预,结合 TGFβ/PDGF-BB(两种经典 HSCs 活化信号)处理,验证 ATF4 对 HSCs 活化作用。Western blot 与 qPCR 结果显示TGFβ 诱导的间充质标志物FN1、N-cadherin与纤维化标志物α-SMA、COL1A1、COL1A2表达均依赖 ATF4,且 ATF4 过表达可放大TGFβ 效应。ISRIB 可显著抑制 TGFβ/PDGF-BB 诱导的 HSCs 活化,且该效应能被 ATF4 过表达挽救,证明 ISRIB 的抗纤维化作用依赖 ATF4。此外,对比肝细胞(AML12),ATF4 对 ECM 基因的调控在 HSCs中更显著,体现出明确的细胞特异性。该实验首次在 HSCs 中证实 ATF4 的促活化作用(图1)。

图1 ATF4是肝星状细胞活化的必要条件
2. HSCs 特异性敲除 ATF4 对小鼠肝纤维化的体内干预效果
为验证 ATF4 在体内肝纤维化进程中的必要性,研究人员构建了 HSCs 特异性 ATF4 敲除小鼠,并通过 CCl₄诱导肝纤维化模型进行验证。与野生型小鼠相比,HSCs-ATF4-KO 小鼠肝组织中,Western blot 与 qPCR 结果显示 CCl₄诱导的间充质标志物FN1、VIM与纤维化标志物α-SMA、COL1A1、COL1A2表达显著降低。天狼星红染色和 Masson 三色染色显示胶原沉积明显减少,羟基脯氨酸定量进一步证实胶原水平下降。同时血清肝功能指标检测显示肝损伤程度减轻。该实验通过细胞特异性敲除模型,在体内证实HSCs 中的 ATF4是肝纤维化的必需因子(图2)。

图2 在体内肝星状细胞特异性耗竭 Atf4 可减轻肝纤维化
3. ATF4 通过增强子调控 COL1A1/LOXL2 等纤维化靶基因转录
研究人员通过 ChIP-qPCR、荧光素酶报告基因实验及 JQ1(增强子抑制剂)干预,验证ATF4 - 增强子 - 靶基因的调控关系。ChIP-seq 可视化显示,TGFβ 处理下 ATF4 可结合 COL1A1/LOXL2 的增强子区域,且这些区域伴随 H3K27ac 富集(COL1A1/LOXL2 为超增强子,CDH2 为典型增强子)。ChIP-qPCR 证实,TGFβ 可增强 ATF4 与靶基因增强子的结合,而 JQ1(抑制 BRD4、阻断增强子活性)可显著抑制该结合;荧光素酶报告基因实验显示,含 COL1A1 增强子的报告基因活性依赖 TGFβ 与 ATF4,JQ1 可完全阻断该活性。明确了 ATF4 通过结合增强子直接调控纤维化靶基因(图3)。

图3 ATF4通过增强子依赖机制促进纤维化基因的转录
结 语
该研究针对肝纤维化缺乏有效靶向治疗的临床难题 HSCs活化病理事件为核心,系统揭示了转录因子 ATF4 的非经典促纤维化机制,打破 ATF4 仅调控内质网应激的传统认知,证实其在 TGFβ 等纤维化信号作用下,可通过重塑 H3K27ac 标记的活性增强子景观,优先结合 COL1A1、LOXL2 等相关基因的超增强子 / 典型增强子,直接驱动 HSCs 活化与细胞外基质过度沉积。针对上述有关ATF1对HSCs活化及肝脏纤维化研究,朴衡博迈可快速构建HSCs中ATF4特异性敲低的3D人源化肝脏模型,验证ATF4对HSCs活化以及胶原沉积的作用。明确潜在干预靶点的作用机制,验证靶点在复杂生理条件下的有效性与特异性,减少体内实验的盲目性。朴衡博迈开发的人源化3D肝纤维化模型(NF-HS-2-01)采用成熟的人原代肝实质细胞、肝窦内皮细胞、肝星状细胞与库普弗细胞构建。该模型克服了传统肝类器官成熟度不足与细胞类型单一的缺陷,相比普通2D细胞培养,能更有效地重现肝脏生理微环境,且无种属差异。其细胞活性及代谢能力显著优于传统2D系统,加之建模周期短,可快速应用于高通量药物筛选及靶点功能验证。作为研究慢性肝病发病机制和进行高通量药物筛选的理想工具,朴衡博迈构建的人源化 3D 肝脏模型已成功助力多项研究成果发表于 Hepatology、Gut、Cellular & Molecular Immunology、Cancer Communications 等国际高水平期刊。

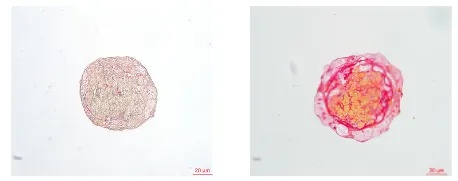
图1 朴衡博迈肝脏生理模型(左)
与肝脏纤维化模型(右)天狼猩红染色结果

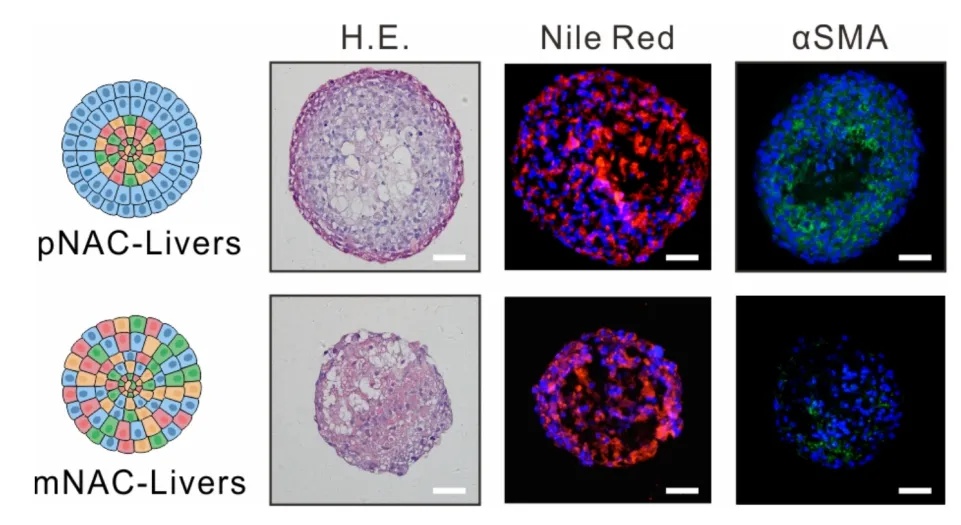
图2 朴衡博迈3D MASH模型
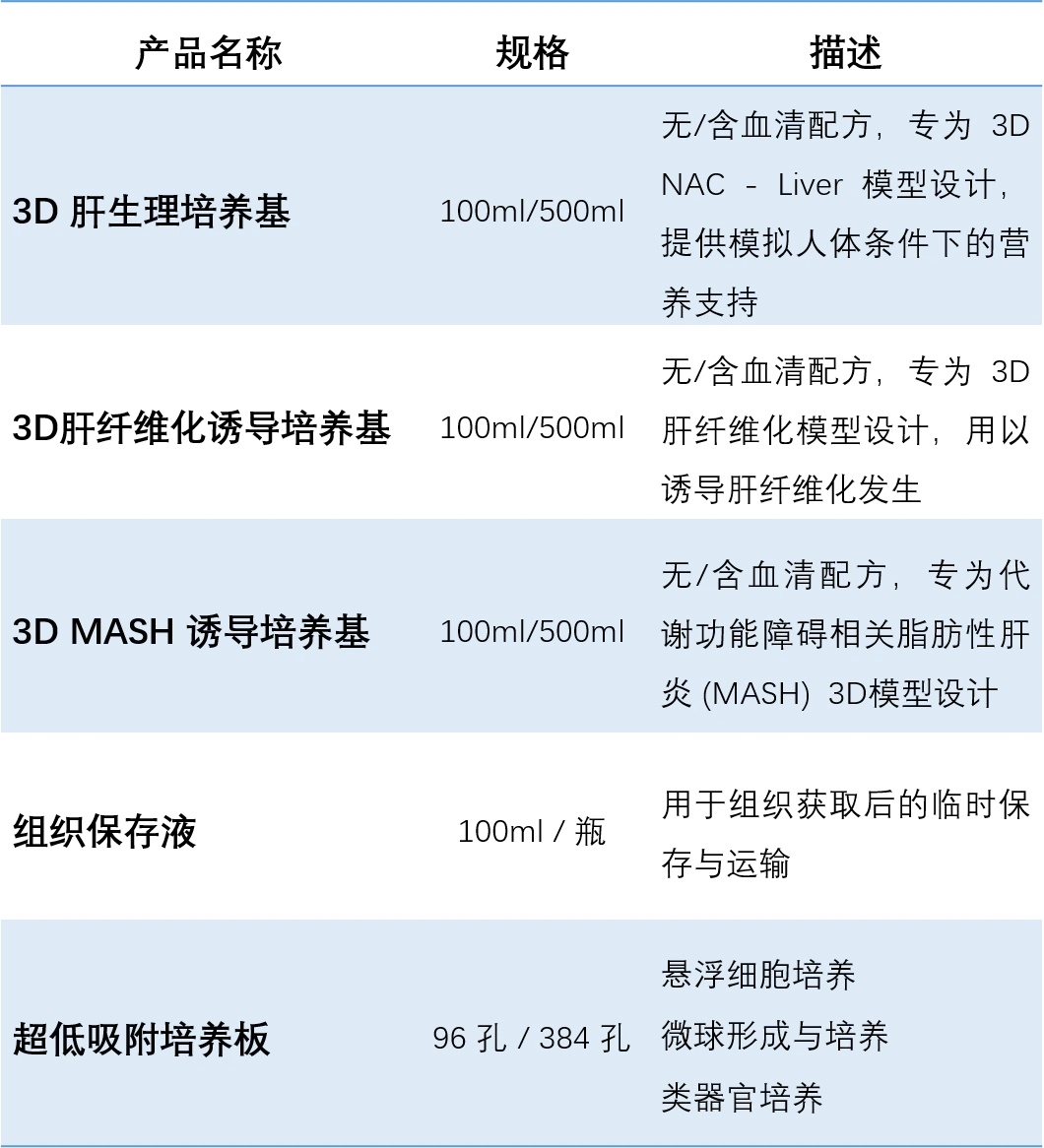
产 品 目 录

服 务 列 表

