上海市浦东新区康安路388弄2号615单元
新闻动态
朴衡最新成果:利用NAC-Organ 3D 培养技术平台加速CAR-Macrophage细胞的高通量体外筛选
CAR-T细胞、TILs细胞等免疫细胞治疗方法作为一种新兴的治疗手段在肿瘤治疗领域展现出了巨大潜力,目前免疫细胞治疗方法在药效评估方面存在一些局限性,人源化体外3D培养模型通过减少动物实验和利用人源性组织,避免了物种差异带来的偏差,特别适用于患者特异性的肿瘤研究和传染病机制探索,为抗肿瘤药物研发提供更高效、更精准的研发工具。此外,体外3D培养技术可以构建多器官系统和长期培养,为研究药物在多个器官间的相互作用及长期毒性效应提供了独特的优势。
嵌合抗原受体巨噬细胞(CAR-M)凭借其卓越的免疫浸润能力和高效的靶向杀伤效能,在实体瘤治疗领域展示了显著的临床潜力。为了进一步促进CAR-M疗法的临床转化与应用,开发高效、精准的评估体系以快速量化其浸润与杀伤性能显得尤为重要。这不仅有助于深入理解CAR-M的作用机制,还能为优化治疗方案、提升患者预后提供坚实的数据支持。
近日,朴衡博迈团队、鲲石生物团队与张硌教授团队三方联合,利用朴衡博迈自主研发的3D NAC-Organ类器官技术平台,建立了适用于鲲石生物设计研发的靶向HER2 CAR-M细胞的高通量体外筛选系统,并在这种人源化体外3D模型中评估了CAR-M对实体瘤的靶向募集、浸润和杀伤能力。这一研究不仅证实了CAR-M细胞疗法在实体瘤治疗中的潜力,也为未来的临床应用提供了重要的药效筛选平台。 科研团队的最新研究成果,题为“3D DNA Origami Assembled Spheroid for Evaluating Cytotoxicity and Infiltration of Chimeric Antigen Receptor Macrophage (CAR-M)”的论文,已在国际知名学术期刊《Communications Biology》上发表。

在本研究中,研究团队设计并构建了一种靶向HER2的CAR基因盒。使用高效基因转导能力的病毒载体将CAR-HER2基因导入人单核细胞来源的巨噬细胞(hMDM),和小鼠巨噬细胞系(RAW264.7)中,并实现了超过85%的CAR阳性表达。研究显示,无论是hMDM CAR细胞还是RAW CAR细胞,虽然两者之间存在一定的表型差异,但均展现出促炎表型(图1),这种特性有利于增强HER2 CAR-M细胞在肿瘤微环境中的活性,进而提高其对肿瘤细胞的杀伤效率。
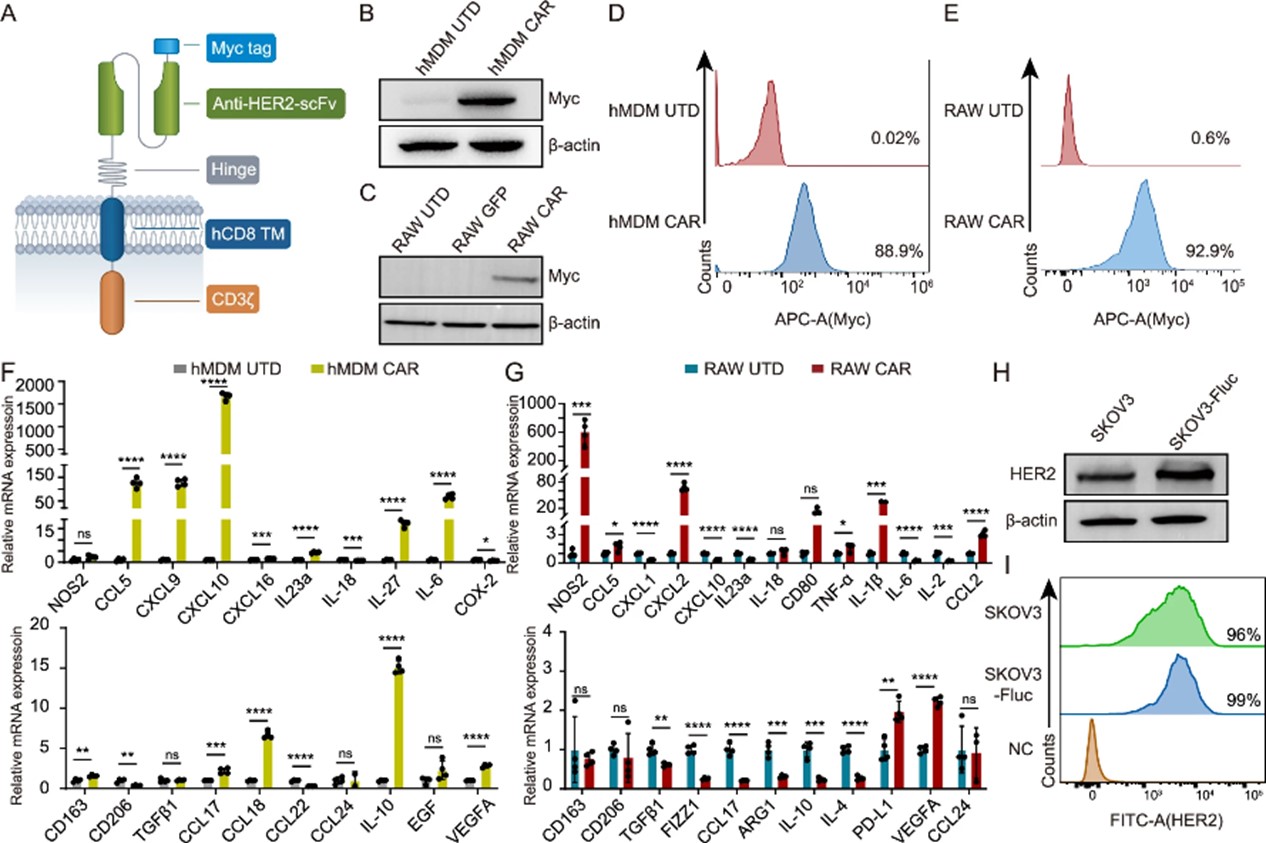
图1 CAR-M的构建及表型鉴定
为了评估HER2 CAR-M细胞对HER2阳性细胞的吞噬与杀伤效能,本研究选用高表达HER2的卵巢癌细胞系SKOV3及带有萤火虫荧光素酶标记的SKOV3-fluc作为靶标。使用双色标记策略对CAR-M细胞和靶标细胞分别染色,共培养后评估了CAR-M细胞的吞噬效率。流式实验结果显示,CAR-M细胞组(包括hMDM CAR细胞和RAW CAR细胞)对SKOV3细胞的吞噬效率上均显著高于对照组。
进一步,采用LDH释放实验和萤火虫荧光素酶活性检测评估了HER2 CAR-M的杀伤效力。前者基于检测受损细胞释放的LDH酶活性来量化细胞毒性,后者通过监测荧光素酶活性的降低程度来反映细胞存活状态的变化。结果一致表明:HER2 CAR-M细胞对SKOV3-Fluc细胞的杀伤效果显著增强。
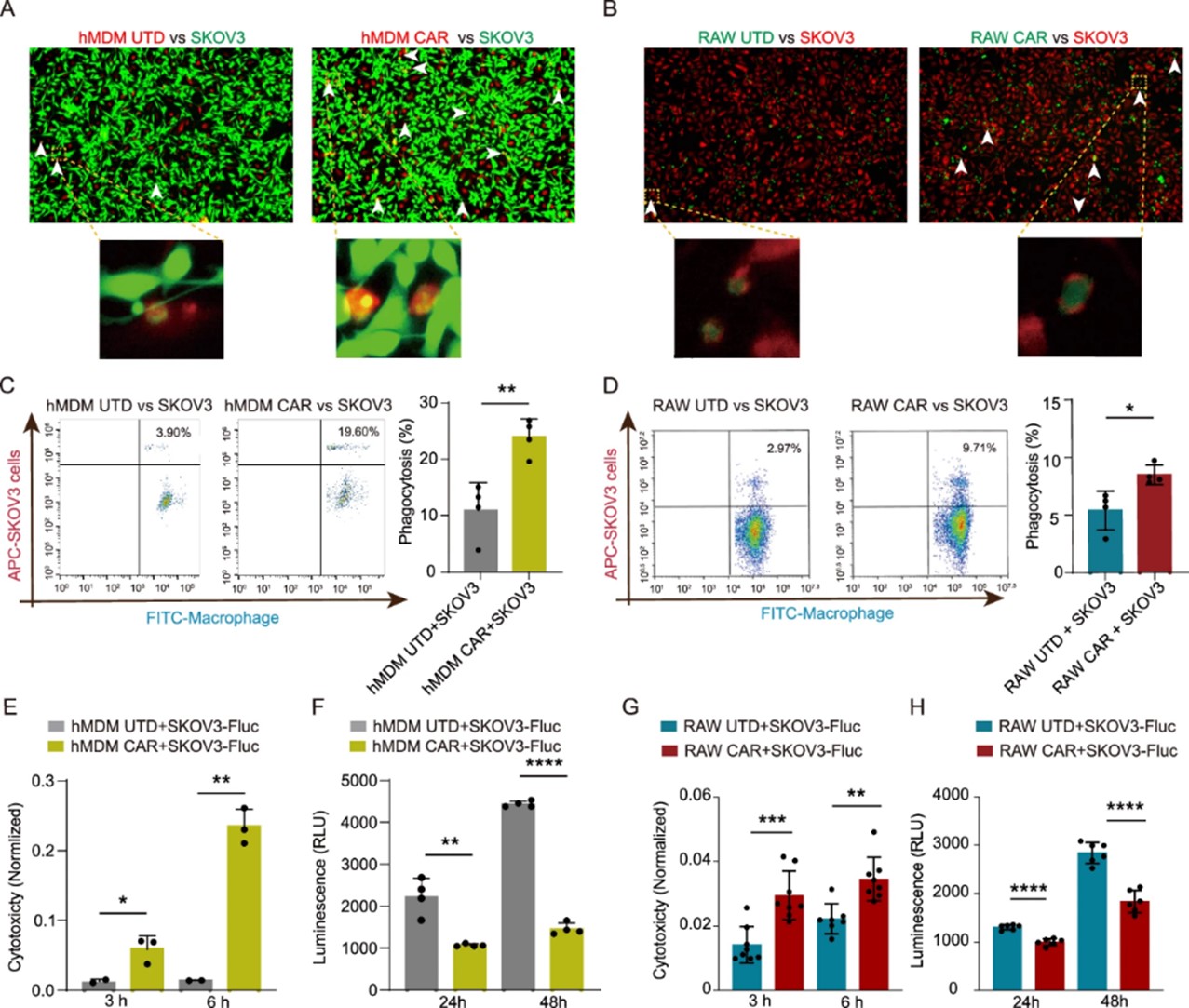
图2 CAR-M在2D水平的靶向吞噬和细胞毒性作用
团队应用自主研发的NAC-Organ技术构建了基于SKOV3细胞的3D卵巢癌实体瘤微球(NAC-Solid Tumor),该模型具有较高的稳定性和活性,并且无需基质胶支撑,可与免疫细胞长期共培养,使免疫细胞能够主动侵入肿瘤模型(图3)。通过活细胞实时成像系统观察到,巨噬细胞能够有效渗透进入该肿瘤模型。这种三维肿瘤模型成功模拟了肿瘤与免疫细胞之间的动态相互作用,是评估CAR-M细胞的靶向浸润和杀伤效能的强有力平台。
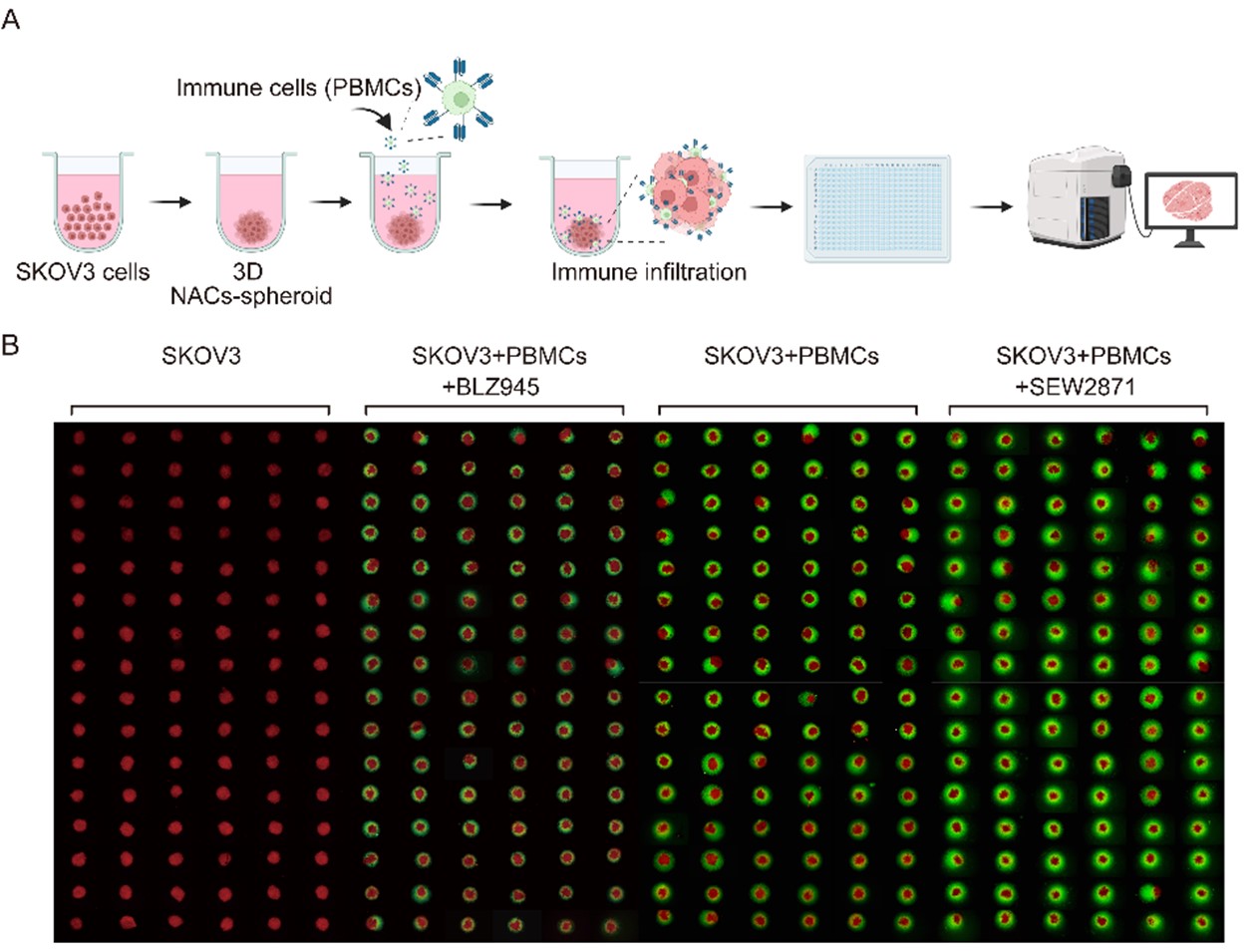
图3 PBMC与3D肿瘤微球高通量互作模型
为了验证HER2 CAR-M细胞对实体瘤的识别、渗透和细胞毒性,团队利用卵巢癌SKOV3-Fluc细胞构建了三维肿瘤球体模型。通过将UTD-M细胞和HER2 CAR-M细胞与肿瘤球体共培养,评估了不同效应细胞与靶细胞比例(E/T)和作用时间下的浸润和细胞毒性作用。结果显示,HER2 CAR-M在不同E/T比例下均能有效浸润肿瘤球体,尤其在E/T比为10:1时效果最为显著。相比之下,UTD-M细胞仅表现出轻微的靶向性,难以深入肿瘤球体内部。在E/T比为10:1时,HER2 CAR-M细胞对实体瘤球体的细胞毒性显著高于UTD-M细胞(图4),并且这种浸润能力和细胞毒性的提高随着时间的推移逐渐增强(图5)。
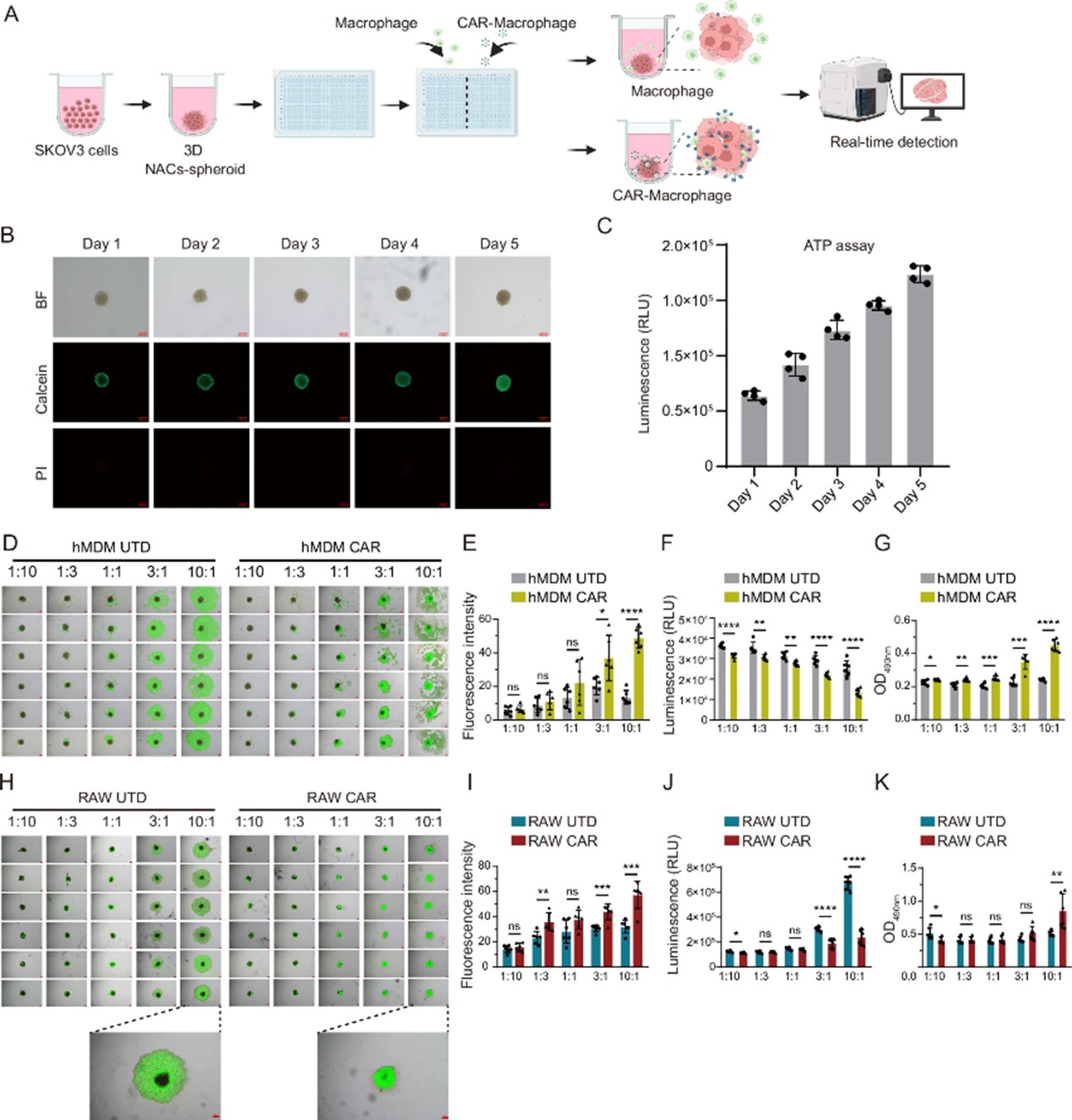
图4 CAR-M细胞对3D肿瘤微球的靶向、浸润能力评估
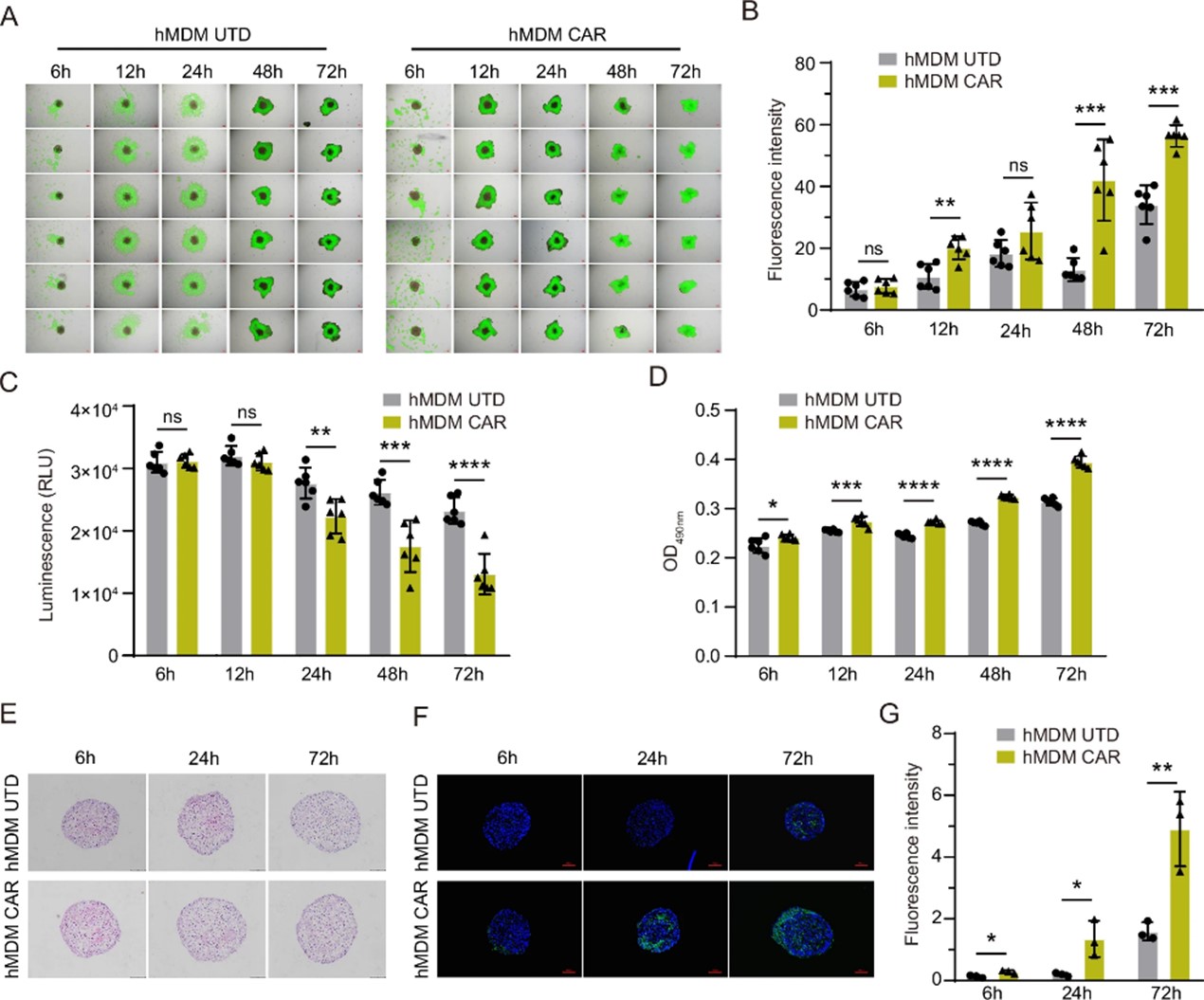
图5 CAR-M细胞对3D肿瘤微球的靶向、浸润能力评估
本研究通过结合NAC-Organ技术和CAR-M细胞疗法,在三维卵巢癌模型中系统评估了CAR-M细胞对实体瘤的靶向浸润和杀伤能力,提出了一种创新的解决方案来应对实体瘤治疗的复杂挑战。研究结果不仅为CAR-M细胞的临床应用奠定了坚实的科学基础,还为个性化医疗和精准治疗提供了新的思路和方法。
