上海市浦东新区康安路388弄2号615单元
新闻动态
专访|可检测频率低至0.001%抗原特异性T细胞,华东师大团队基于「DNA折纸术」开发新型多聚体用于精准免疫监测,将进行产业落地
更新时间:2022-08-15 08:37:00点击次数:3087次
7 月10 日,第一届合成生物学竞赛——创业赛 SYNBIO HIVE 在深圳理工大学(筹)明珠校区拉开帷幕,来自未融资组的华东师范大学裴昊团队开发的“基于 Dorimer 技术的精准免疫监测”项目获得技术突破奖。该项目是由华东师范大学化学与分子工程学院、医学合成生物学研究中心及上海交通大学转化医学研究院联合创建。
据了解,这种 Dorimer 技术增强了对于低亲和力抗原特异性 T 细胞受体的结合能力,相较于其他多聚体技术,其能够检测到更多 T 细胞,且具有高价态、高灵敏度、低背景染色等优势,是针对抗原特异性免疫细胞精准监测的一种新工具。目前,这项研究已经以“Nanoscale organization of two-dimensional multimeric pMHC reagents with DNA origami for CD8⁺ T cell detection”(基于 DNA 折纸技术的二维 pMHC 多聚体用于 CD8⁺ T 细胞检测)为题发表在Nature Communications上。

▲图|(来源:Nature Communications)
“所谓 Dorimer 技术,其实是一种基于 DNA 折纸技术而开发的新型 pMHC 多聚体技术,可实现对抗原特异性 T 细胞的高灵敏检测,能够应用于精准免疫监测,新抗原的高通量筛选以及新 TCR-T 细胞疗法发开发等领域。”该论文的通讯作者、华东师范大学化学与分子工程学院裴昊教授告诉生辉。

▲图|华东师范大学化学与分子工程学院裴昊教授(左)(来源:受访者)
从南京大学本科毕业后,裴昊进入中国科学院上海应用物理研究所攻读博士学位,师从中国科学院院士樊春海教授。博士毕业后,他进入美国纽约大学 Ned Seeman 课题组从事博士后研究工作。2015 年,他回国进入华东师范大学化学与分子工程学院担任研究员并成立课题组,研究方向为 DNA 纳米技术、生物传感器、细胞表面工程化及 DNA 自组装等。
截至目前,裴昊已在Nature Machine Intelligence、Nature Communications、JACS、Angewandte Chemie International Edition、Advanced Materials等期刊上发表论文 110 余篇,被引 8000 余次,H-index 为 46。此外,他还曾获 2021 年中国分析测试协会科学技术一等奖,拥有 4 项中国专利。
该论文第一作者孙越洋是华东师范大学在读博士,她本科毕业于浙江工业大学化学工程学院,2017 年进入裴昊教授课题组攻读硕士学位并于 2019 年转为博士研究生,研究方向为免疫治疗伴随诊断技术的开发。她曾在Nature Communications等期刊上发表 4 篇研究论文,已申请 2 项中国专利。

▲图|华东师范大学化学与分子工程学院孙越洋博士(来源:受访者)

“基于 DNA 折纸技术开发新型 pMHC 多聚体”
如今,癌症已经成为威胁全球健康的重大公共卫生问题。数据显示,2020 年全球新发癌症 1929 万例。免疫细胞疗法逐渐成为了癌症治疗的新“风口”,并涌现出 CAR-T、TCR-T 等一系列技术路线。
在治疗过程中,针对免疫反应的监测是评估免疫细胞疗法有效性和安全性的重要指标。通过对抗原特异性 T 细胞的精准检测,可以跟踪患者在免疫治疗前、治疗中和治疗后对于免疫疗法的反应情况。就现阶段而言,pMHC 多聚体技术是检测抗原特异性 T 细胞的一个“金标准”,其分子识别机制为肽-主要相容性复合物(pMHC)与 T 细胞表面受体(TCR)的特异性结合。
据介绍,目前已经实现商业化的 pMHC 多聚体技术有四聚体、五聚体和葡聚体等产品,但现阶段仍存在一些不足。比如,四聚体(低价态 pMHC 多聚体)难以进行全范围的 T 细胞的检测;而葡聚体(高价态 pMHC 多聚体)虽然能够和 T 细胞进行更好的结合,但也会出现背景染色增强等问题。“所以,我们开始思考是否有一种技术,既能精准调控 pMHC 多聚体,又能在增加价态的同时解决高背景染色问题,最终,我们采用了DNA 折纸技术(DNA Origami)。”孙越洋说道。
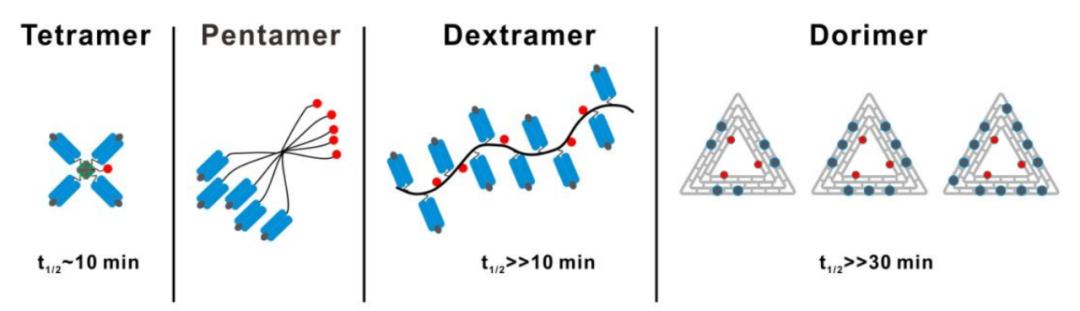
▲图|四聚体、五聚体、葡聚体和 Dorimer 多聚体结构示意(来源:受访者)
“在生命科学领域,DNA 是遗传物质,但它其实也是一种很好的生物材料。”裴昊指出,“由于 DNA 具有严格的 A(腺嘌呤)-T(胸腺嘧啶)和 C(胞嘧啶)-G(鸟嘌呤)配对原则,因此,通过对序列编程就可以在纳米尺度下把 DNA 分子作为一种生物材料‘折叠’成任意形状和大小的结构,而这就是 DNA 折纸技术,能够在纳米尺度对 DNA 进行精准控制。”
DNA 折纸技术可以编程 DNA 形状并对双链进行修饰,因此可实现对 pMHC 分子的位置、数目、朝向等的精准控制。“此外,由于我们采用的二维 DNA 折纸是一种较大的平面结构,这种结构能够促进支架上 pMHC 分子和 T 细胞表面受体的结合,这就克服了因价态升高而导致背景染色增强问题。”孙越洋表示。
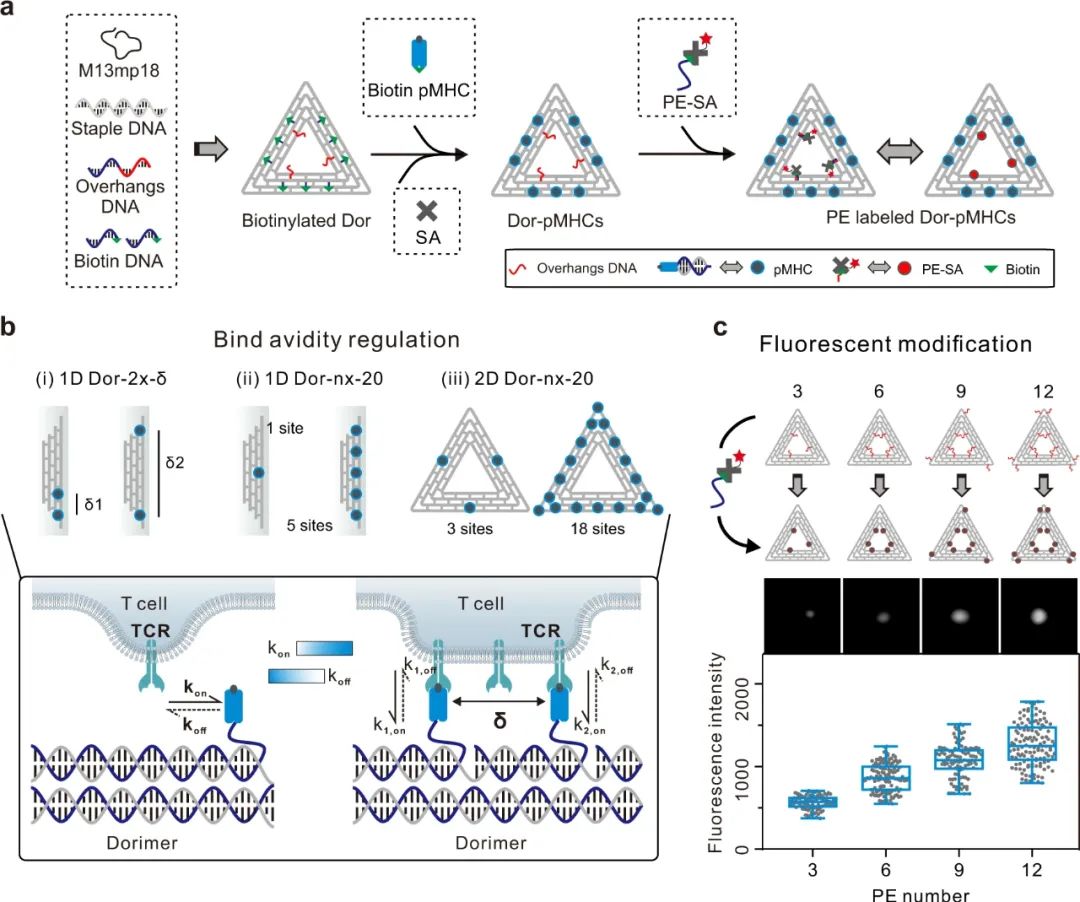
▲图|通过 DNA 折纸技术对 pMHC 分子进行纳米级组装(来源:Nature Communications)
在这项研究中,裴昊团队首先制作了边长约 120 nm 的三角形 DNA 折纸作为二维支架,然后对 pMHC 分子进行纳米级组装,构建出基于 DNA 折纸的 pMHC 多聚体(Dorimer)。在检测自身免疫性 CD8⁺ T 细胞试验中,由于 TCR 的亲和力较低,自身免疫 T 细胞一般很难在外周血中直接检测到。他们将这种 Dorimer 多聚体应用于在非肥胖糖尿病(NOD)小鼠的脾中鉴定自身免疫 CD8⁺ T 细胞,试验发现 Dorimer 多聚体可以检测到 17.4% 的特异性的 CD8⁺ T 细胞,对比之下,四聚体和葡聚体则只能分别检测到 0.97% 和 7.80% 的 CD8⁺ T 细胞。
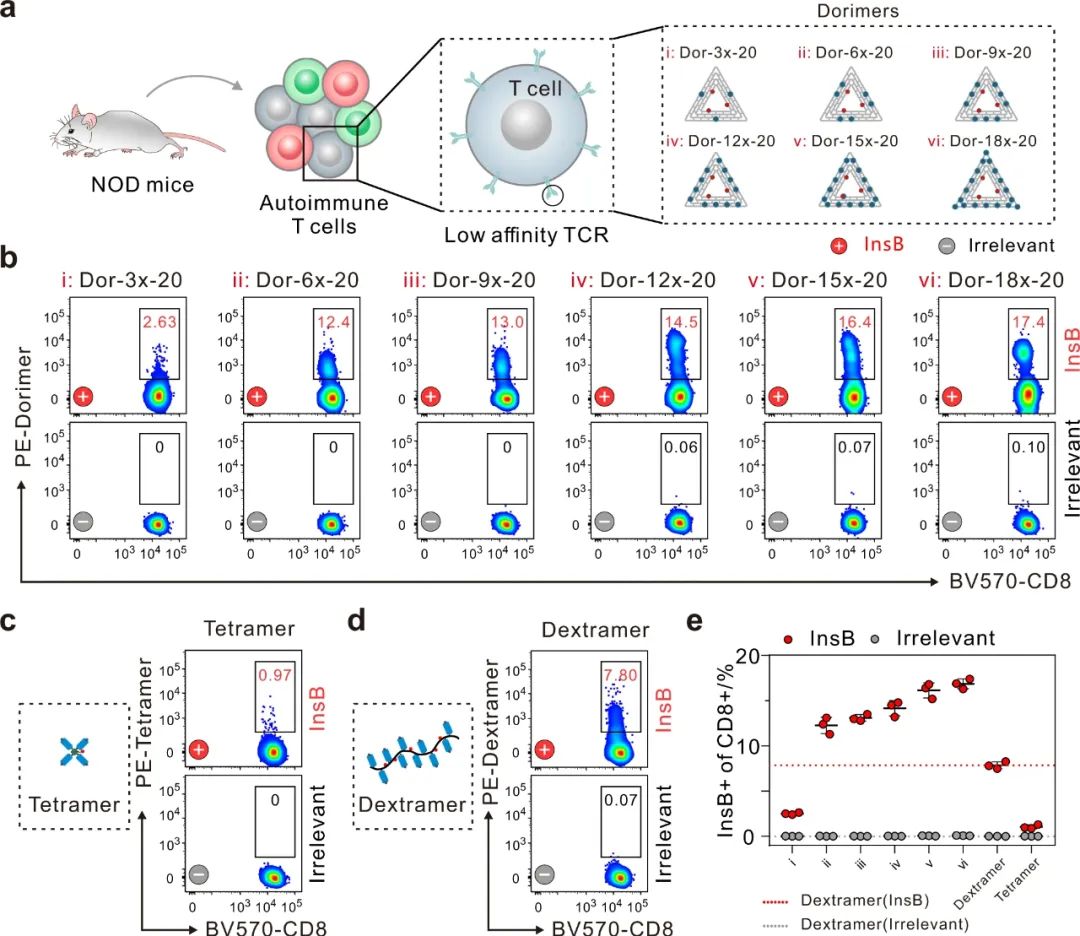
▲图|使用 Dorimer 技术检测自身免疫 CD8⁺ T 细胞(来源:Nature Communications)
谈及开展这项研究的初衷,裴昊介绍道,“我们课题组专注于 DNA 折纸技术的研究,随着研究的不断深入,我们开始思考 DNA 折纸技术能否来解决当前临床所面临的各种问题。随着近年来癌症治疗领域中免疫疗法的热度颇高,一次偶然的机会我们关注到了 pMHC 多聚体技术,通过研究发现,pMHC 多聚体技术的核心点其实是支架组装,当时我们便想能否利用 DNA 折纸技术来代替目前的支架组装技术。”
“基于这个想法我们开展了研究,通过试验发现在 DNA 折纸上可以精确地组装 pMHC 分子且 pMHC 的价态和间距都精准可控,并且其与抗原特异性 T 细胞的结合亲和力和结合稳定性可以通过改变 pMHC 价态或间距来进行调节。”他说道。
据介绍,这种基于 DNA 折纸技术开发的 pMHC 多聚体技术(Dorimer 多聚体)不仅可以应用于传染病和癌症疫苗领域,还能广泛应用于细胞免疫疗法、移植免疫、自身免疫疾病等基础研究和临床领域开发中,为临床前和临床免疫学研究提供新的解决方案。

“寻求广泛合作,未来计划把 Dorimer 技术进行产业转化”
谈及这项研究所面临的挑战,在孙越洋看来,主要是来自跨学科领域的研究。“我们在 DNA 折纸技术领域的的经验较为丰富,挑战在于把 DNA 折纸技术应用于生物免疫反应检测。首先,我们的对于免疫反应方面的理论知识积累略微薄弱,此外,研究过程还涉及到大量生物实验,我们对于实验操作技能、仪器使用技能等都较为欠缺,所以前期研究工作的开展比较缓慢。”她说道。
对于这两个方面挑战,裴昊、孙越洋及团队展开科研攻关:
其一,理论知识方面。“首先,我们开展了大量的文献调研,无论是 pMHC 多聚体的背景知识还是发展现状都进行了全方面的学习;然后,搭建课题的整个框架,一步一步地解决问题,并通过试验不断验证我们技术的可行性和优越性等,最终目标是将其应用于抗原特异性 T 细胞免疫检测。”孙越洋说。
其二,实验技能方面。“在丰富知识的同时,我们也参加了很多相关的学术会议以及仪器公司举办的技能培训等,以此来不断地学习和强化自身实验操作技能。”她表示,“最终,我们的知识、技能都实现了较大提升,借助试验不断发现问题并解决问题,依托对已有技术的调研来反复优化 Dorimer 技术。”
“鉴于初步试验取得了比较理想的结果,我们开始尝试把 Dorimer 多聚体和两款已经商业化的主流 pMHC 多聚体进行对比。”裴昊说道。四聚体技术是最早开发出来的一种 pMHC 多聚体技术,后来,为了能够检测到更低亲和力的抗原特异性 T 细胞新开发出了葡聚体技术,这也是目前最前沿的 pMHC 多聚体技术。“相较于四聚体和葡聚体,Dorimer 多聚体技术具有高价态、高灵敏度、低背景染色以及可检测低亲和力 T 细胞等优势,是现阶段其他 pMHC 多聚体技术所难以替代的。而这,也树立了我们在这个领域继续深入研究的信心。”他补充说。
对于下一步的研究动向,孙越洋介绍说,“接下来我们计划把 Dorimer 技术结合DNA 编码技术和人工智能技术,搭建起一个深度免疫学检测平台。”比如,通过结合高通量测序技术可以实现高通量筛选,能够对患者体内的T细胞进行大规模检测和分析,这可用来发现新的 TCR,进而有望开发出新一代 TCR-T 细胞疗法。
对此,裴昊也补充说,“开发新 TCR-T 细胞疗法的核心是发现新抗原,然后针对抗原设计新的 TCR,进而改造或创造新的 T 细胞用于治疗癌症。我们正在开发‘DNA Barcode’技术,通过一次筛选就可以得到更多的免疫组学信息,加速发现新抗原并用于开发新 TCR-T 细胞疗法;同时,利用人工智能的方法预测 pMHC 多聚体与 TCR 之间的相互作用,以此来优化试验过程、缩短新 TCR-T 细胞疗法的开发过程。在人工智能方面,我们已经有了很好的合作伙伴,我们已和长期从事分子科学及人工智能方面研究的朱通教授课展开了紧密合作。”
谈及这项研究的产业化落地,“我们目前还处于科学研究阶段,下一步将准备进行产业转化。过渡到产业阶段会涉及到如生产成本、制造工艺等的挑战,同时也会面临资金、人才等的挑战。”孙越洋表示,“所以,未来我们把技术进行产业化落地还需要资金、人才、平台等多方面的协作与支持。”
关于产业层面,在裴昊看来,“四聚体和葡聚体等技术目前均有公司进行开发,其主要是面向科研试剂领域,但这个领域的市场份额并不是很大。我们发现Dorimer 技术可以作为 TCR-T 细胞疗法新抗原发现的一项底层技术。所以,我们计划基于 pMHC 多聚体技术建立深度免疫检测平台,未来将开发 TCR-T 的新管线。”他指出。
“目前,我们的产业化思路已经梳理得较为清晰了。第一阶段,首先搭建深度免疫检测平台,对外提供科研服务,而这就相当于是为广大生物学家或公司提供了平台技术。第二阶段,寻找细胞治疗领域的专家一起合作,共同开发新 TCR-T 细胞疗法的管线。”裴昊说道。
参考资料:
1.https://doi.org/10.1038/s41467-022-31684-8
2.https://www.ecnu.edu.cn/info/1094/60639.htm
