上海市浦东新区康安路388弄2号615单元
新闻动态
文献分享|脂肪来源SVF自组装“多功能骨类器官”:成骨、血管化、免疫调节三位一体,破解骨修复难题!
更新时间:2026-02-11 11:09:00点击次数:346次
骨骼是人体的支撑核心,但大骨缺损、骨折不愈合、骨坏死等复杂骨科疾病,一直是临床治疗的棘手难题。传统骨移植疗法存在显著局限:自体骨供区有限、手术创伤大,异体骨易引发免疫排斥,而单纯干细胞移植又难以解决血管化不足、炎症微环境失衡等问题。
近年来,类器官技术与骨组织工程的结合为治疗带来新希望。脂肪组织来源的基质血管部分(SVF),因获取便捷、细胞成分丰富,成为骨类器官构建的潜力细胞源。它包含脂肪间充质干细胞(ADSCs)、内皮祖细胞(EPCs)、周细胞及免疫细胞等异质性细胞群,天然具备参与骨修复的多重潜能。
2025年11月,来自中国人民解放军总医院第四医学中心骨科研究所、贵州医科大学、锦州医科大学附属第一医院的团队在《Bioactive Materials》(IF=20.3)上发表了题为Stromal vascular fraction self-assembles vascularized osteogenic organoids with immunomodulatory functions的文章,首次利用 SVF 的自组装能力,构建出兼具成骨、血管化、免疫调节三重功能的骨类器官。该类器官在裸鼠骨折模型中表现出优异的修复效果,为复杂骨疾病治疗提供了全新策略。

01. SVF 骨类器官的制备与特性验证
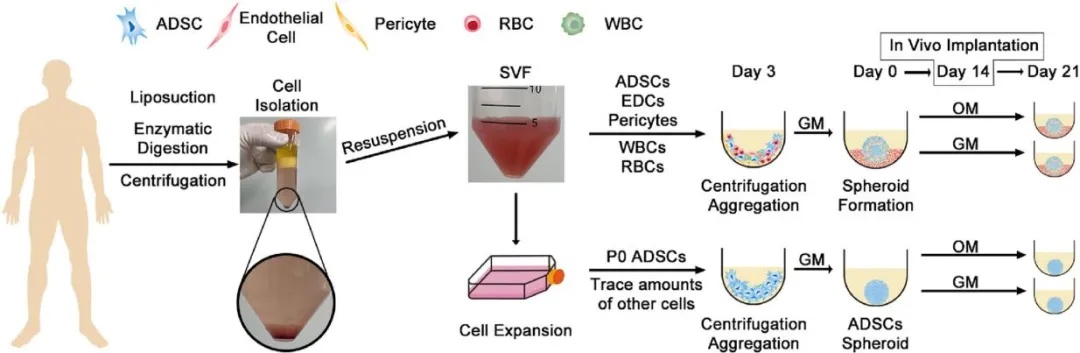
研究团队从50例接受抽脂手术的患者脂肪组织中,通过酶解、离心、过滤等步骤分离获得 SVF,同时从相同供体的SVF中培养纯化出ADSCs作为对照。将SVF和ADSCs分别接种到超低吸附96孔板,经3天自发聚集形成球体后,分为生长培养基(GM)组和成骨诱导培养基(OM)组,持续培养至 21 天。
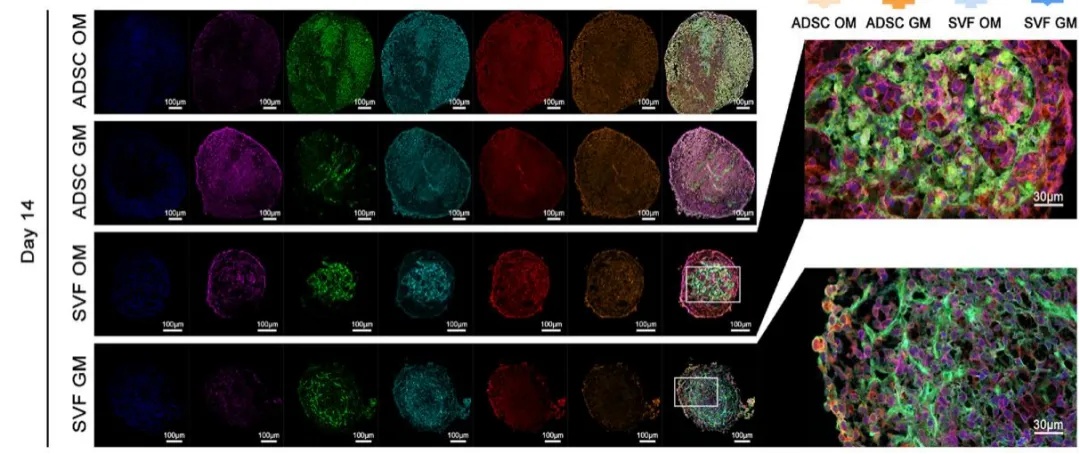
多色免疫荧光共定位结果显示:SVF类器官在培养 0、7、14、21 天(GM/OM条件)下,能自发形成有序空间结构 —CD31⁺内皮细胞构成管状网络,PDGFR⁺周细胞沿血管平行分布,CD68⁺巨噬细胞定位于外周,CD44⁺脂肪间充质干细胞弥漫分布,在14天趋于成熟,模拟天然微血管与免疫分区;而ADSC类球体无 CD31⁺结构,细胞紧密堆积,缺乏空间组织性。
02. SVF 骨类器官的成骨、血管化及免疫调节能力
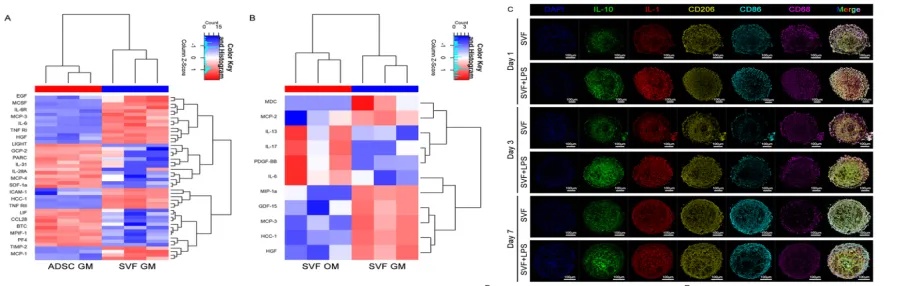
研究人员通过成骨染色、血管标志物检测及炎症刺激实验,系统验证了SVF类器官的三重核心功能:成骨方面,经ALP、ARS染色及qPCR证实,SVF类器官(尤其OM组)7 天即出现矿化结节,RUNX2、OPN等成骨基因表达显著高于ADSC组,固有成骨潜能更优;血管化方面,多色免疫荧光与基因检测显示,SVF类器官无需外源因子即可自发形成CD31⁺内皮细胞管状网络,PDGFR⁺周细胞沿血管分布,CD31、VEGF表达量为ADSC组的2.5 倍以上,GM条件更利于血管网络维持;免疫调节方面,蛋白芯片与LPS刺激实验表明,SVF类器官可分泌120余种细胞因子,炎症刺激后呈现“先促炎(IL-1、TNF-α升高)后抗炎(IL-10、TGF-β主导)”的时间节律,且外周富集M1巨噬细胞、核心聚集M2巨噬细胞,形成空间极化布局,而ADSC组无明显免疫调节响应。
03. 体内验证:无需预诱导,高效修复骨折
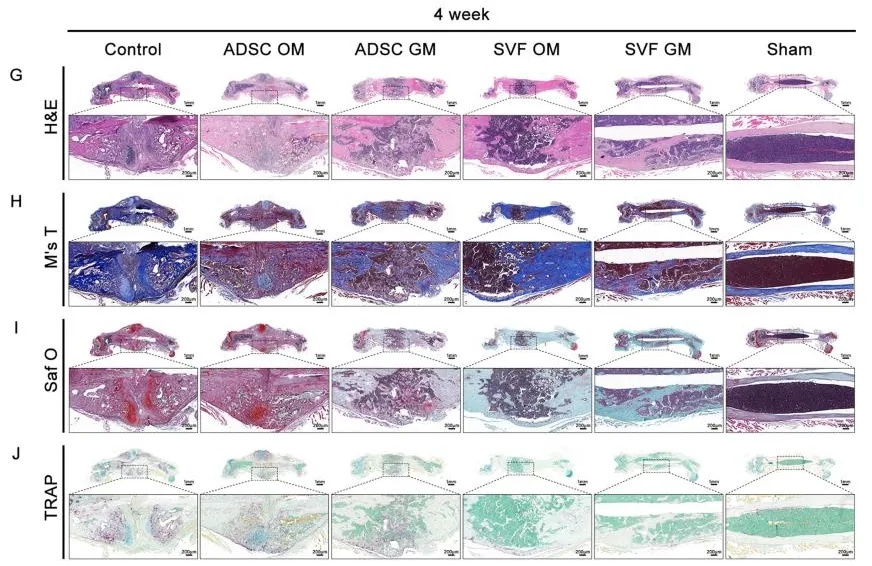
为验证临床转化潜力,研究团队在裸鼠股骨骨折模型中移植SVF类器官(GM/OM 组)和ADSCs球体,4周后通过Micro-CT、组织染色及免疫荧光检测发现:SVF组骨折间隙模糊、骨痂成熟,骨体积分数(BV/TV)和骨矿物质密度(BMD)显著高于ADSC组及空白对照组,其中无成骨预诱导的SVF-GM组修复效果最优;在组织学层面,SVF组骨结构连续、胶原排列有序、破骨细胞数量少,人源OCN染色证实供体细胞存活并参与骨形成,愈合质量接近正常骨组织。
该研究创新性地利用 SVF 的自组装能力,构建出无需外源支架、无需预诱导的多功能骨类器官,完美解决了传统骨组织工程中“成骨-血管化-免疫调节”难以协同的核心痛点。其优势在于:
1. 细胞来源便捷:脂肪组织易获取,无需复杂扩增培养;
2. 功能全面:集“成骨+血管化+免疫调节”于一体,匹配天然骨修复微环境;
3. 临床转化潜力大:可即时制备移植,无需体外成骨诱导,安全性和实用性更高。
随着类器官技术的发展,SVF来源的骨类器官有望成为复杂骨缺损、骨折不愈合等疾病的新型治疗方案,为骨组织工程的临床转化开辟新路径。
近年来,类器官技术与骨组织工程的结合为治疗带来新希望。脂肪组织来源的基质血管部分(SVF),因获取便捷、细胞成分丰富,成为骨类器官构建的潜力细胞源。它包含脂肪间充质干细胞(ADSCs)、内皮祖细胞(EPCs)、周细胞及免疫细胞等异质性细胞群,天然具备参与骨修复的多重潜能。
2025年11月,来自中国人民解放军总医院第四医学中心骨科研究所、贵州医科大学、锦州医科大学附属第一医院的团队在《Bioactive Materials》(IF=20.3)上发表了题为Stromal vascular fraction self-assembles vascularized osteogenic organoids with immunomodulatory functions的文章,首次利用 SVF 的自组装能力,构建出兼具成骨、血管化、免疫调节三重功能的骨类器官。该类器官在裸鼠骨折模型中表现出优异的修复效果,为复杂骨疾病治疗提供了全新策略。
Bioactive Materials
IF=20.3

Bioactive Materials ( IF 20.3 ) Pub Date : 2025-11-18
DOI: 10.1016/j.bioactmat.2025.10.030
原文链接:
https://doi.org/10.1016/j.bioactmat.2025.10.030
01. SVF 骨类器官的制备与特性验证
研究团队从50例接受抽脂手术的患者脂肪组织中,通过酶解、离心、过滤等步骤分离获得 SVF,同时从相同供体的SVF中培养纯化出ADSCs作为对照。将SVF和ADSCs分别接种到超低吸附96孔板,经3天自发聚集形成球体后,分为生长培养基(GM)组和成骨诱导培养基(OM)组,持续培养至 21 天。
多色免疫荧光共定位结果显示:SVF类器官在培养 0、7、14、21 天(GM/OM条件)下,能自发形成有序空间结构 —CD31⁺内皮细胞构成管状网络,PDGFR⁺周细胞沿血管平行分布,CD68⁺巨噬细胞定位于外周,CD44⁺脂肪间充质干细胞弥漫分布,在14天趋于成熟,模拟天然微血管与免疫分区;而ADSC类球体无 CD31⁺结构,细胞紧密堆积,缺乏空间组织性。


图1 实验流程示意图与多色免疫荧光染色图
02. SVF 骨类器官的成骨、血管化及免疫调节能力
研究人员通过成骨染色、血管标志物检测及炎症刺激实验,系统验证了SVF类器官的三重核心功能:成骨方面,经ALP、ARS染色及qPCR证实,SVF类器官(尤其OM组)7 天即出现矿化结节,RUNX2、OPN等成骨基因表达显著高于ADSC组,固有成骨潜能更优;血管化方面,多色免疫荧光与基因检测显示,SVF类器官无需外源因子即可自发形成CD31⁺内皮细胞管状网络,PDGFR⁺周细胞沿血管分布,CD31、VEGF表达量为ADSC组的2.5 倍以上,GM条件更利于血管网络维持;免疫调节方面,蛋白芯片与LPS刺激实验表明,SVF类器官可分泌120余种细胞因子,炎症刺激后呈现“先促炎(IL-1、TNF-α升高)后抗炎(IL-10、TGF-β主导)”的时间节律,且外周富集M1巨噬细胞、核心聚集M2巨噬细胞,形成空间极化布局,而ADSC组无明显免疫调节响应。

图2 SVF衍生类器官和ADSC球体
诱导的差异性蛋白分泌及炎症反应
03. 体内验证:无需预诱导,高效修复骨折
为验证临床转化潜力,研究团队在裸鼠股骨骨折模型中移植SVF类器官(GM/OM 组)和ADSCs球体,4周后通过Micro-CT、组织染色及免疫荧光检测发现:SVF组骨折间隙模糊、骨痂成熟,骨体积分数(BV/TV)和骨矿物质密度(BMD)显著高于ADSC组及空白对照组,其中无成骨预诱导的SVF-GM组修复效果最优;在组织学层面,SVF组骨结构连续、胶原排列有序、破骨细胞数量少,人源OCN染色证实供体细胞存活并参与骨形成,愈合质量接近正常骨组织。

图3 体内治疗效果组织学染色图
总 语
该研究创新性地利用 SVF 的自组装能力,构建出无需外源支架、无需预诱导的多功能骨类器官,完美解决了传统骨组织工程中“成骨-血管化-免疫调节”难以协同的核心痛点。其优势在于:
1. 细胞来源便捷:脂肪组织易获取,无需复杂扩增培养;
2. 功能全面:集“成骨+血管化+免疫调节”于一体,匹配天然骨修复微环境;
3. 临床转化潜力大:可即时制备移植,无需体外成骨诱导,安全性和实用性更高。
随着类器官技术的发展,SVF来源的骨类器官有望成为复杂骨缺损、骨折不愈合等疾病的新型治疗方案,为骨组织工程的临床转化开辟新路径。
